TJOD
İstanbul Şubesi



Değerli Meslektaşlarım,
Ekim
-
Kasım
2019
Bülteninde,
geçen
yıl
röportajını
yayınladığımız
Yavuz
Ceylan
Hoca’dan
ülkemize
bir
çok
başka
yenilikle
beraber
modern
obstetrik
bakımı
getiren
Besim Ömer Paşa ve ilk doğumevi ile ilgili yazısıyla başlıyoruz.
Yazılarımıza
gelince
giderek
popülerleşen
ve
kanımca
gereğinden
fazla
kullanılan
bir
test
olan
anti
Müllerian
hormon’un
polikistik
over
tanı
kriteri
olarak
ve
menopoz
yaşı
öngörüsünde
rolünü
değerlendiren
iki
makaleyle
başlıyoruz.
Sinem
Ertaş’ın
tercüme
ettiği
ilk
makalede
kullanılan
ve
Sinem’in
“olasılık
oranı”
diye
tercüme
ettiği
istatistik
terimlerden
likelihood
ratio’dan
daha
önce
bahsetmiştim.
Bu
makalede
bazılarınızın
ilk
kez
duyabiliyor
olacağı
bir
diğer
terim
ise
Summary
receiver
operating
characteristic
curve
(SROC).
Makele
de
ROC
açıklandığı
için
o
detaya
girmeden,
summary
ROC’un
tanısal
testleri
değerlendiren
çalışmalardaki
verileri
bir
araya
getirerek
meta-analiz
yaparken
oluşturulan
ROC
olduğunu
ve
aynı
şekilde
yorumlandığın
söyleyebiliriz.
Ancak,
bu
ROC’un
da
güvenilirliği
birleştirilen
çalışmaların
ne
kadar
benzer
olduğuna
dayandığından
bu
örnekte
biraz
sınırlı
kanaatimce.
Bu
karışık
görünen
makalenin
ana
fikri
AMH’nın
polikistik
over
morfolojisi
yerine
kullanımının
poliksitik
over
sendromu
tanısını
daha
iyi
hale
getirebileceği
ama
belirlenen
bir
eşik
değer
yok
maalesef.
Berna
Aslan’ın
tercüme
ettiği
ikinci
AMH
makalemizde
ise
AMH
düzeyi
ile
menopoz
yaşı
arasında
bir
ilişki
olmakla
beraber
ne
tek
bir
ölçümün ne de aralıklı ölçümlerdeki değişimin menopoz yaşını öngörmeyi henüz sağlamadığı.
Cihan
Kaya’nın
tercüme
ettiği
morsellasyon
hakkındaki
güncel
yazı
güzel
bir
özet
ve
bence
en
önemli
vurguladığı
şey
karar verme sürecine hastanın da dahil edilmesi. Tabii ki bu sürecin dokümantasyonu önemli olacaktır.
Engin
Çelik’in
hazırladığı
onkoloji
makalemizde
kadınlarda
onkolojik
tarama
hizmetleri
için
güncel
önerilerin
derlemesini
göreceksiniz.
Muhtemelen
siz
de
benim
gibi
bunları
her
okuyuşunuzda
aynı
verilere
bakarak
aynı
ülkelerin
kurumlarının
nasıl
bu
kadar
farklı
sonuçlara
vardığına
şaşıracaksınız
bir
kez
daha.
Bu
güzel
özet
fikir
vermekle
beraber
yasal
açıdan
ülkemizde
Sağlık
Bakanlığı’nın
kılavuzlarını
en
azından
hastalarımız
ile
paylaşmakla
yükümlü
olmalıyız.
Sonuçta
herkes
çalıştığı yerdeki ruhsat otoritesine tabi kalıyor.
Cenk
Yaşa’nın
hazırladığı
makale
Kanada
Jinekoloji
ve
Obstetrik
Derneği’nin
Ürojinekoloji
de
mesh
kullanımı
ile
ilgili
güncel
önerileri
var.
Bu
kez
de
iki
ülkenin
(İngiltere
ve
Kanada)
yaklaşımları
arasındaki
fark
dikkat
çekici.
Kanadalıların
düşünce
şeklini
sadece
bu
makale
özelinde
değil
genel
olarak
beğendiğimi
ve
açık
fikirli
bulduğumu
söyleyebilirim
ama
Kanada’da eğitim almış birisi olarak bu karşılaştırmada pek tarafsız olamayabilirim :)
Son
yazımızda
Hakan
Erenel,
gebelik
öncesi,
gebelik
sırası
ve
puerperiumda
antifosfolipid
sendromu
yönetimini
anlatan
bir
makale
hazırladı.
Her
şeyin
ne
kadar
detaylandığını
ve
komplike
vakaların
yan
dal
uzmanlığı
düzeyinde
zaman
ayırarak
elde
edilebilecek
bilgi
ve
deneyim
olmadan
ideal
şekilde
yönetilmesinin
mümkün
olmayabileceğini
düşündüm
okurken.
Bu
kadar
farklı
alanda,
bu
kadar
farklı
detayda,
bu
kadar
çok
üretim
varken
hepsini
tam
detayda
takip
etmek
herhalde mümkün olamaz artık.
Son
olarak
Mayıs
2020
toplantımız
için
ameliyat
videolarınızı
ve
sunumlarınızı
beklediğimizi
hatırlatmak
istiyorum.
Hem
videolar hem tüm öneri ve yorumlarınızı bekliyoruz.
Gelecek bültenimizde görüşene kadar sağlık ve mutlulukla kalın.
Saygılarımla,
Dr. Barış Ata
barisata@ku.edu.tr
Kadın Hastalıkları ve Doğum Anabilim Dalı Koç Üniversitesi Tıp Fakültesi
TJODist
Bülteni



Kasım 2019

TJOD
İstanbul Şubesi



DUYURU:
Değerli meslektaşlarımız,
Mayıs
2020
’de
“Jinekolojik
Endoskopi”
konulu
aylık
bilimsel
toplantımızı
videolar
üzerinden
tartışmalarla
interaktif
bir
şekilde
yapmayı
planlıyor
ve
endoskopi
yapan
üyelerimizin
kendi
deneyimleri ile katkıda bulunmasını arzu ediyoruz.
Tartışmacı
ve
sunucu
olarak
katılmak
isteyen
tüm
üyelerimizden
8
dakikayı
geçmeyen
editlenmiş
operasyon
videolarını
vakanın
kısa
bir
özeti
ile
beraber
31
Mart
2020
’ye
kadar
bize
ulaştırmasını
rica
ediyoruz.
Video
dosyalarını
wetransfer
kullanarak
barisata@ku.edu.tr
adresine
gönderebilirsiniz.
Organizasyon
komitesi
ile
seçeceğimiz
videoların
sahiplerini
toplantıda
videolarını
göstererek
operasyonu
tanıtmaya
ve
deneyimli
cerrahlardan
oluşan
bir
panelle
fikir
alışverişinde
bulunmaya
davet edeceğiz.
Operasyonların
endikasyon
ve
türleri
ile
ilgili
bir
sınırlamamız
olmamakla
beraber,
program
farklı
operasyonların
farklı
basamaklarını
içerecek
bir
şekilde
organize
edeceğimiz
için
videolarınız
mutlaka
bir
operasyonu
baştan
sona
göstermek
zorunda
değildir.
Operasyonun
sadece
bir
aşamasına
da
odaklanmış
videolar
da
gönderilebilir.
Örneğin;
laparoskopik
histerektomide
vaginal
kafa girilmesi, frozen pelviste retroperitona ilk giriş aşaması veya bir komplikasyonun onarımı gibi.
Sizlerin sunumlarını görmeyi ve hepberaber birbirimizden öğrenmeyi bekliyoruz.
Toplantı Eş Başkanları
Dr. Barış Ata - Dr. Mete Güngör


TJODist
Bülteni


TJOD
İstanbul Şubesi


TJODist
Bülteni
TJOD İstanbul Yönetim Kurulu
Dr. Ahmet Gül (Başkan)
Dr. Recep Has (2. Başkan)
Dr. Funda Güngör Uğurlucan (Sekreter)
Dr. Veli Mihmanlı (Sayman)
Üyeler (Soyadı Sırası)
Dr. Halil Aslan
Dr. Barış Ata
Dr. Burcu Özmen Demirkaya
Dr. Albert Kazado
Dr. Engin Oral
Dr. Abdullah Tüten
Dr. Gökhan Yıldırım
Bülten Kurulu (Soyadı Sırası)
Editörler
Dr. Barış Ata
Dr. Engin Oral
Editöryal Kurul Üyeleri
Dr. Engin Çelik
Dr. Berna Aslan Çetin
Dr. Nadiye Köroğlu Duğan
Dr. Hakan Erenel
Dr. Cihan Kaya
Dr. Sinem Ertaş
Dr. Engin Türkgeldi
Dr. Cenk Yaşa


TJOD
İstanbul Şubesi
1862
(Prof.
Yeşim
Işık
Ülman
1861,
Prof.
Dr.
Aykut
Kazancıgil
1863
tarihini
vermektedir)
yılında
doğan
Besim
Ömer
(Akalın),
Askerî
Tıbbiye’yi
1885
yılında
birincilikle
bitirdikten
sonra
bir
süre
Haydarpaşa
Askerî
Tatbikat
Hastanesi
ve
Serfice’de
askerî
hekim
olarak
çalıştı.
Geçirdiği
tifodan
sonra,
açılan
sınavı
kazanarak
Mekteb-i
Tıbbiye-i
Şâhâne’de
Fenn-i
Kibale
(Ebelik
Bilgisi)
hocası
Mehmed
Vahit
Bey’in
yardımcılığına
başladı.
İleri
görüşlü
ve
aydın
bir
hekim
olan
Mehmed
Vahit
Bey,
Besim
Ömer’in
Fenn-i
Velâde
(Doğum
Bilgisi)
eğitimi
alması
için
1887
yılında
Paris’e
gitmesine
ön
ayak
oldu.
Besim
Ömer’in
öğrenci
olduğu
yıllarda
Türkçe
eğitim
yapılan
Askerî
Tıbbiye’de
Birgivîzâde
Mehmed
Nuri
Bey’in
Lucién
Penard’dan
çevirdiği
“Rehnümâ-i
Kavabil”
(Ebelerin
Kılavuzu)
ve
İbrahim
Lütfi
ile
arkadaşları
tarafından
1881
yılında
Friedrich
Wilhelm
von
Scanzoni
(1821-1891)’den
çevrilen
“Fenn-i
Velâde”
adlı
kitaplar
okutuluyordu.
Ancak
hem
Mülkî
(Sivil),
hem
de
Askerî
Tıbbiye’de
bir
doğum
kliniği
yoktu.
Dolayısıyla
eğitim,
Tıbbiye’de
ve
1838
(1843?)
yılında
kurulmuş
olan
Ebelik
Mektebi’nde tamamen teorikti ve fantom üzerinde yapılıyordu.
O
yıllarda
ise
Fransa’da
obstetrik
parlak
bir
dönem
yaşamaktaydı.
Gebe
izlemi,
normal
ve
patolojik
doğumlar
ve
yeni
doğan
bakımı
fakülte
hastanelerinde
yapılıyor,
eğitim
uygulamalı
olarak
veriliyordu.
Besim
Ömer,
Étienne
Stéphane
Tarnier
(1828-1897)’in
adının
verilmiş
olduğu,
Prof.
Pierre-Constant
Budin
(1846-1907)
ile
Prof.
Adolphe
Pinard
(1844-1934)’ın
çalışmakta
olduğu
klinikte
derslere
devam
etti
ve
kısa
sürede
Pinard’ın
asistanı
oldu.
Budin’in
öğrencilere,
doğum
kliniklerine
devam
ettikleri
sürece
otopsiye
ve
diseksiyona
girmeyeceklerine
dair
yemin
ettirdiği
kliniklerde
antisepsi
ve
asepsiye
çok
dikkat
ediliyordu
ve
prematüre
bakımı
ileri
düzeydeydi.
Besim
Ömer
burada
1888
yılında,
Türkiye’de
bu
konudaki
ilk
yayın
olan
“Zayıf
ve
Vakitsiz
Doğan
Çocuklara
Dikkatler:
Küvöz
ve
Gavaj”
adlı
bir
monografi
yayınladı.
Fakat
aynı
yıl,
Fenn-i
Kibale
hocası
Mehmed
Vahit
Bey’in
ölümü
dolayısıyla,
onun
görevini
yapmak
üzere
geri
çağrıldı.
Gelemeyeceğini
bildiren
Besim
Ömer’in
gerekçesinin
Askerî
Tıbbiye
yönetimince
kabul
edilmesi
üzerine
4,5
yıl
daha
kalan
Besim Ömer 13.Kasım.1891’de yurda döndü ve görevine başladı.
Gördüklerini
ve
öğrendiklerini
uygulayabileceği
ve
uygulamalı
eğitim
verebileceği
modern
bir
doğum
evi
açmak
isteyen
Besim
Ömer,
bu
konuda
II.
Abdülhamid’e
pek
çok
kez
dilekçe
yazdı,
ancak
hepsi
reddedildi.
Besim
Ömer
bu
çabalarını
anılarında
şöyle
anlatmaktadır:
“..Nezd-i
Şâhânede
(padişahın
nazarında)
vilâdethane
(doğum
evi),
bir
“piçhane”
gibi
telâkki
(kabul)
ediliyordu..”
Bunun
nedeni
de,
Osmanlı
ailelerinde
doğumların
ev
ve
konaklarda
yapılıyor
olmasıydı.
Evlerinde
doğum
yapamayanlarsa,
evlilik
dışı
gebe
kalanlar
ya
da
fahişeler
gibi
gizli
doğum
yapmak
zorunda
kalanlardı.
Sonunda
Besim
Ömer
1892
yılında,
Sirkeci
Demirkapı’da
“Vilâdethane”sini
gizlice
açtı.
Bu
süreci,
“Doğum
Tarihi”
(1932)
adlı
kitabında
şöyle
anlatmaktadır:
“..1892
yılında
Demirkapı’da,
Saray-ı
Hümâyûn
(Topkapı
Sarayı)
dahilinde
vâki
(olan)
Taşkışla’da
bulunan
Mekteb-i
Tıbbiye-i
Şâhâne
civarında,
nebatat
(bitki)
bahçesi
arkasında,
Sur-u
Sultanî
(Topkapı
Sarayı
surları)’ye
muttasıl
(bitişik),
üç
oda
ve
bir
sofadan
ibaret
iki
katlı
küçük
bir
bina
adeta
gizli
bir
Seririyât-ı
Vilâdiye
(Doğum
Kliniği)
hâline
getirilerek,
o
zamana
kadar
tamamen
nazarî
(teorik)
olan
Fenn-i
Kibale
ve
Emrâz-ı
Nisâ
(Kadın
Hastalıkları)’nın
bir
dereceye
kadar
amelî
(pratik,
uygulamalı)
olarak
tedrisine
(öğretilmesine)
ve
manken
(fantom)
üzerinde
mümâresatına
(alıştırma)
ve
ameliyât-ı
velâdiye
(doğum
ameliyatları)
iradesine


TJODist
Bülteni

TÜRKİYE’NİN İLK DOĞUM EVİ - VİLÂDETHANE
Yazan: Dr. Yavuz Ceylan

TJOD
İstanbul Şubesi
(yapılmasına) başlanılmıştı. Memleketimizde ilk Seriyât-ı Vilâdiye işte burasıdır..”
Besim
Ömer,
halkı
burada
doğum
yapmaya
özendirmek
için
konferanslar
verdi,
gazetelerde
yazılar
yazdı.
Son
sınıf
öğrencileri
altılı
gruplar
hâlinde
nöbet
tutuyor,
lohusalara
et
suyu
ve
süt
veriliyordu.
Modern
küvözler
vardı,
parçalayıcı
girişimler
hatta
sezaryen
yapılıyordu.
Örneğin,
“Hanım
Kızlara
Mahsus”
adlı
derginin
Kasım
1900
tarihli
83-285
no’lu
sayısında,
Boğazkesen
6
no’lu
evde
oturan
Ömer
kızı
Hatice’nin,
dört
beş
gün
süren
doğum
eyleminden
sonra
doğuramayıp
“hayat
ile
memat”
(yaşamla
ölüm)
arasında
kaldıktan
sonra
Vilâdethane’ye
yetiştirildiğini,
“tezâyuk-ı
havsala”
(pelvis
uygunsuzluğu)
nedeniyle
“hazz-ı
cenin”
ameliyatı”
(cenin
kesme,
yırtma)
yapılarak
hayatının
kurtulduğunu
ve
18
gün
sonra
“iade-i
âfiyetle”
yâni
iyileşerek
evine
döndüğünü
yazmaktadır.
Hastanın
18
gün
yatmış
olması,
yapılanın
embryotomiden
çok
sezaryen
olduğunu
düşündürmektedir.
Ancak
tüm
bunlar
kolay
olmadı.
Hatta
Besim
Ömer,
Vilâdethane’nin
kapısında
tutucu
bir
grubun
sırtına
taş
atmasına
rağmen,
içeri
girmesini
söyleyenlere,
“-Bunların
önünde
bir
adım
bile
geri
adım
atmam..”
diyerek
dimdik durmuştur.
Vilâdethane’nin
akıbetine
gelince;
Vilâdethane,
17
yıl
başarıyla
hizmet
verdikten
sonra
1909
yılında
Kadırga’da
açılan
Ebe
Okulu’na
taşındı.
Tapusu
Büyükşehir
Belediyesi’ne
ait
olan
bina,
önce
Belediye
Bahçeler
Müdürlüğü
olarak
kullanıldıktan
sonra
İETT’nin
hurda
makine
ve
lastik
deposu
olarak
kullanıldı
ve
giderek
harabeye
döndü.
Zaman
içinde
yeri
unutulan
Vilâdethane
binası,
1997
yılında
Prof.
Dr.
Ayten
Altıntaş
ve
Yrd.
Doç.
Dr.
Oğuz
Ceylan
tarafından
keşfedilip
tıp
tarihine
kazandırıldı.
Günümüzdeyse,
İslâm
Bilim
ve
Teknoloji
Tarihi
Müzesi
kompleksine
dahil
edilmiş
olup
önüne
Besim
Ömer’in
bir
büstünün
ya
da
en
azından
bir
plaket
konacağı günleri hasretle beklemektedir.
1940
yılında
Ankara’da
bir
asthma
nöbeti
sonucu
hayatını
kaybeden
Besim
Ömer’in
kabrinin
yerinin
bilinmiyor
oluşu,
tarihimize
gösterdiğimiz
vefasızlığın
bir
nişânesi
olduğunu
belirtmek
istiyorum.
Yolumuz
Gülhane
Parkı
civarına düştüğünde, bu büyük insanı hatırlamayı, saygılarımızı ve hayır dualarımızı sunmayı esirgemeyelim.
Kaynakça
AKALIN, Besim Ömer Ord. Prof. Dr: “Doğum Tarihi” Ahmet İhsan Matbaası İstanbul, 1932
ALTINTAŞ, Ayten; CEYLAN, Oğuz Yrd. Doç. Dr.: “Vilâdethane” Tombak Dergisi 17: 26-30, 1997
KAZANCIGİL, Aykut Prof. Dr.: “Ölümünün 40. Yılında Besim Ömer Paşa (1863-1940)
Dirim Dergisi 9-10: 237-47 İstanbul, 1980


TJODist
Bülteni

TJOD
İstanbul Şubesi
Özet
Amaç: Anti Müllerian Hormon (AMH) ile ilgili yapılan önceki meta-analizde bu testin Polikistik Over Sendromu (PKOS)
tanısında başlangıç tanısal testi olarak yaralı olabileceği gösterilmiştir. Bu çalışma mevcut meta-analizi güncellemek ve
AMH testinin tanısal yeterliliğini değerlendirerek Rotterdam Kriterlerinde polikistik over morfoloji kriterinin yerini
alabilirliğini ortaya koymayı amaçlamaktadır.
Metod: İki bağımsız araştırmacı PubMed, Cochrane Library ve Web of Science veri tabanlarını kullanarak sistematik
olarak ‘Anti-Müllerian Hormon’ ve ‘Polikistik Over Sendromu’ anahtar kelimeleri ile ilgili makaleleri belirlemişlerdir. 31
Temmuz 2018’e kadar olan tüm çalışmalar değerlendirilmiştir. Rastgele-etki modeli kullanılmıştır ve subgrup analizi ve
meta regresyon kullanılarak olası heterojenite kaynakları belirlenmiştir. Her çalışmanın metodolojik kalitesi QUADAS-2 ve
funnel plot asimetri testi ile değerlendirilmiştir.
Sonuçlar: Dahil etme kriterlerine göre 29 çalışma meta-analize katılmıştır. Sadece AMH’ın PKOS tanısında kullanılması
ile sensitivite, spesifisite ve tanısal olasılık oranı (DOR) sırasıyla 0.76 (95%CI 0.71-0.81), 0.86 (95%CI 0.82-0.90) ve 20
(95%CI 12-33) idi. AMH, PKOS tanısında Polikistik Over Morfolojisi (PKOM) yerine kullanıldığında sensitivite, spesifisite
ve tanısal olasılık oranı (DOR) sırasıyla 0.93(95%CI 0.89-0.96), 0.99 (95%CI 0.95-1.00) ve 1634 (95%CI 217-12324) idi.
PKOS tanısında SROC eğrisi altındaki alan (AUC) sadece AMH için ve PKOM yerine AMH’ın kullanılması ile sırasıyla
0.88 (95% CI 0.85-0.91) ve 0.97 (95% CI 0.95-0.98) olarak hesaplanmıştır, bu istatistiksel olarak anlamlıdır
(Z=4.89,P<0.01).
Sonuç: Rotterdam kriterlerinde polikistik over morfolojisi (PKOM) yerine AMH’ın kullanılması polikistik over sendromu
tanısında daha doğru tanısal etkiye sahiptir.
Anahtar kelimeler: Anti-Müllerian hormon, polikistik over sendromu, polikistik over morfolojisi, biyomarker, meta-analiz.
GİRİŞ
Polikistik over sendromu (PKOS) kadın infertilitesine neden olan yaygın endokrin bozukluklardan biridir. Reprodüktif
yaştaki kadınlardaki diğer komplikasyonları insülin direnci, obezite ve kardiyovasküler problemler ve birçok hayati
sorunlardır. Üreme çağındaki kadınların %5-10’ununu etkileyen bu hastalık, seks hormonlarındaki dengesizliklerden ve
ayrıca genetik ve çevresel faktörlerden kaynaklanmaktadır. Ayrıca PKOS adölesanlarda da görülebilmektedir. PKOS’un
temel klinik özellikleri androjen fazlalığı (hirsutizm ve/veya hiperandrojenizm (HA)) ve over disfonksiyonu (oligo-
anovulasyon (OA)) ve/ veya polikistik over morfolojisidir (PKOM). Heterojen kliniğinden dolayı uluslararası standart bir
tanısal yöntem yoktur.
Önerilen birçok tanısal kriterlerin değerlendirilmesi sonrasında 2003 yılında Rotterdam kriterleri uluslararası olarak kabul
edilmiştir. Bu kriterlerde PKOS tanısında mevcut kriterlerden en az ikisinin olması gerekmektedir: OA, klinik ve/veya
biyokimyasal HA bulguları ve diğer etiolojilerin yokluğunda PKOM olmasıdır. PKOM; (2-9 mm boyutlarında) her overde en
az 12 folikül ve /veya ultrasonda artmış over hacmi (>10 mL) olarak tanımlanmıştır.
Geleneksel ultrason tanısında kaçınılmaz problemler bulunmaktadır, hem ultrasonu yapan kişiye bağlı gelişen sübjektif
değerlendirme ve giderek ilerleyen teknoloji nedeniyle artık ultrason değerlendirmesinde çok daha küçük foliküllerin tespit
edilebilmesi yeni tanısal kriter ihtiyacını doğurmuştur.


TJODist
Bülteni
POLİKİSTİK OVER SENDROMUNDA BİYOMARKER OLARAK ANTİ-MÜLLERİAN
HORMONUN TANISAL DEĞERİ: GÜNCEL META-ANALİZ
Özetleyen: Dr. Sinem Ertaş

Link: https://bit.ly/34BLS5L
Diagnostic value of anti-müllerian hormone as a biomarker for polycystic ovary syndrome: a meta-analysis
update Yang Zhao, B.S2*, Yinlong Zhao, Ph.D.3*, Chunpeng Wang, Ph.D.4, Zhenzhen Liang, Ph.D.5, Xin Liu, Ph.D.
Endocr Pract. 2019 Aug 15

TJOD
İstanbul Şubesi
Anti-Müllerian Hormon (AMH); transforming growth faktör beta (TGF beta) ailesinden dimerik bir glikoproteindir.
Kadınlarda AMH büyük oranda preantral ve antral over foliküllerinde yer alan granüloza hücrelerinden salgılanmaktadır.
Bu hormonun yokluğu kadın üreme sisteminin gelişimden sorumludur. AMH erken folikül seçiminin baskılanmasını
sağlamaktadır ve folikül rezervinin erken kaybını engellemektedir. Foliküller büyüdükçe, AMH kademeli olarak
azalmaktadır. Antral folikül sayısı arttıkça AMH üretimi de artmaktadır; bu yüzden PKOM sahip hastalar belirgin olarak
daha fazla serum AMH değerlerine sahiptirler. PKOS’un üç kriterini karşılayan hastalarda yüksek AMH değerleri
saptanmıştır ve PKOM ile yakından ilişkili bulunmuştur. Ayrıca AMH değeri ile hiperandrojenizm ve OA şiddetiyle ilgili
bulunmuştur. AMH’ın yaygın kullanımı ile birlikte over rezervinin belirlenmesinde önemli tanısal bir tarama testi olmuştur
ayrıca PKOS tanısında potansiyel bir biyomarker olarak değerlendirilmektedir.
Birçok çalışmada AMH’ın PKOS tanısında tanısal daha doğru ve geçerli bir biyomarker olduğu gösterilmiştir. PKOS
taramasında AMH’ın sensitivite ve spesifisitesi ile ilgili kesin bir sonuca varılamamıştır. Mevcut çalışmalar prospektif
kohort çalışmalar ile doğrulanmalıdır.
Bu meta-analiz ile birlikte AMH’ın tek başına tanısal etkinliği ve Rotterdam kriterlerinde PKOM tanısında alternatif
kullanılabilirliğinin değerlendirilmesi amaçlanmıştır.
MATERYAL VE METOD
Çalışma stratejisi ve seçim kriterleri
İki bağımsız araştırmacı PubMed, Cochrane Library ve Web of Science veri tabanlarını kullanarak sistematik olarak ‘Anti-
Müllerian Hormon’ ve ‘Polikistik Over Sendromu’ anahtar kelimeleri ile ilgili makaleleri belirlemişlerdir. 31 Temmuz 2018’e
kadar olan tüm çalışmalar değerlendirilmiştir.
Dahil etme kriterleri; (1) orijinal çalışma; (2) 2003 Rotterdam kriterlerine göre PKOS tanısı alan hastalar; (3) PKOS
tanısında potansiyel biyomarker serum AMH; (4) sensitivite ve spesifisitenin ölçülmesi için 2x2 tablolar; (5) eğer iki
çalışma aynı hastaları kapsıyorsa daha büyük popülasyona sahip çalışma baz alınır (6) yayın dili İngilizce olarak
belirlenmiştir; (7) İnsanla ilgili çalışmalar katılacaktır.
Data çıkarma ve kalite değerlendirmesi
Bağımsız iki araştırmacı tarafından araştırmalar değerlendirilmiş, fikir uyuşmazlığı olduğunda üçüncü bir değerlendiriciye
danışılmıştır.
Ayrıca Çalışmaların Tanısal Doğruluk Kalite Değerlendirme (Quality Assessment of Diagnostic Accuracy Studies)
(QUADAS-2) aracı ile dahil edilen tüm literatürün kalitesi değerlendirilmiştir.
İstatistiksel Analiz
Öncelikle eşik etkisi Spearman korelasyon katsayısı ile ölçüldü. Eğer Spearman korelasyon katsayısının p değeri
0.05’den büyük ise; bu bir eşik etkisi olmadığını göstermekteydi. Heterojenite olduğunda, eşik değeri etkisi olmadığında
oluşmaktaydı. Heterojenite testi Cochran-Q test ve I-square istatistik p-değeri ile değerlendirildi. Eğer Cochran-Q test
0.05’den fazla ve I-square istatistik %50’den düşükse; çalışmalar belirgin heterojeniteden uzak olarak kabul edildi.
Modelin sabit etkileri toplam sensitivite (SEN), spesifisite (SPE), pozitif olasılık oranı (PLR), negatif olasılık oranı (NLR),
tanısal olasılık oranı (DOR), ve bunların %95 güvenilirlik aralığı (CI) ile değerlendirilmiştir. Eğer Cochran-Q test 0.05’den
düşük ve I-square istatistik %50’den fazla ise; bu çalışmalarda belirgin heterojenite olduğunu gösterir, böyle durumlarda
rastgele etki modeli kullanıldı. Heterojenitenin nedeninin belirlenebilmesi için meta-regresyon modeli ve subgrup analizleri
yapıldı. Subgrup analizi için 7 ko-değişken sırasıyla; ırk, hasta sayısı, çalışma dizaynı, AMH kit, ortalama yaş, ortalama
BMI ve AMH eşik değeri idi. Toplam sensitivite (SEN), spesifisite (SPE), pozitif olasılık oranı (PLR), negatif olasılık oranı
(NLR), tanısal olasılık oranı (DOR), ve bunların %95 güvenilirlik aralığı (CI) ölçüldü. Tanısal testin doğruluğunu tam olarak
değerlendirmek için SROC ve AUC, %95 güven aralığı (CI) ile değerlendirilmiştir. Tanısal test için AUC 1.0 değerine
yakınsa; bu iyi tanısal yeterlilik anlamına gelir, AUC 0.5’e yaklaştığında bu tanısal testin zayıf olduğunu gösterir.
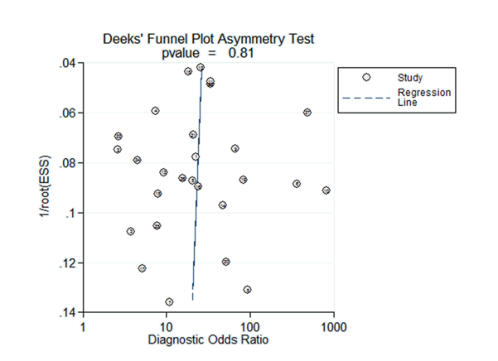
Yayın biası Deek’s funnel plot asimetri testi ile değerlendirildi. Eğer Deeks’ funnel grafiği simetrik ve p-değeri 0.05’ten
fazla ise; bu belirgin yayın biası olmadığı anlamına gelir. Z-test istatistiksel anlamlılığı değerlendirmek için kullanıldı
(p<0.05). Tüm bu analizler Meta-disc software STATA 14.0 ile gerçekleştirildi.


TJODist
Bülteni

TJOD
İstanbul Şubesi
Sonuçlar
Çalışma seçimi
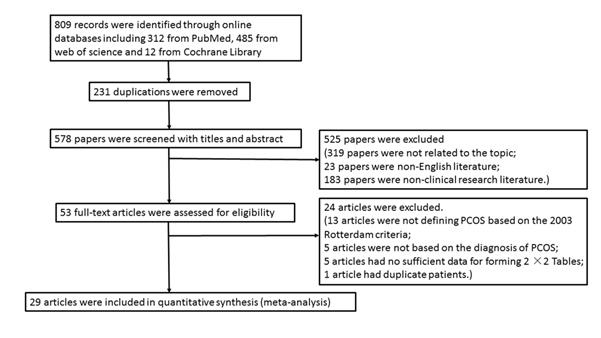
Pubmed’den 312, Web of Science’dan 485 ve Cochrane Library’den 12 olmak üzere toplam 809 makaleye araştırma
stratejisine uygun olarak ulaşıldı. Bunların içinde 231 tekrar olduğu için dışlandı ve 549 makale diğer nedenlerden
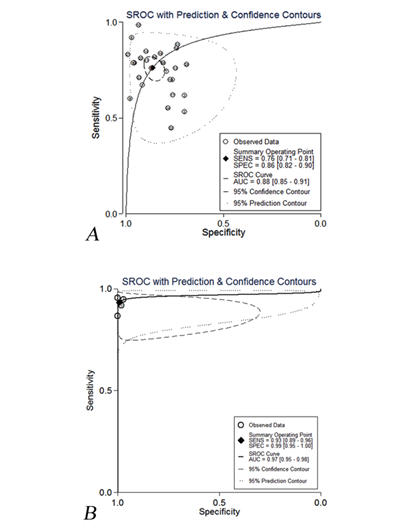
dışlandı. Sonuç olarak 29 makale meta-analize dahil edildi (Figür-1).
Bias riski ve kalite değerlendirmesi
Deeks’ funnel plot asimetri tesi yayın bias riskini değerlendirmek için kullanıldı. Deeks’ funnel grafiği asimetrik ve p-değeri
0.05’ten fazla ise; bu belirgin yayın biası olmadığı anlamına geldi (Figür 2)


TJODist
Bülteni

TJOD
İstanbul Şubesi
Tanısal Doğruluk
(Grup 1; AMH PKOS için tek tanısal test olan grup ve Grup 2; PKOM tanısı için AMH’ı alternatif test olarak kullanan grup)
eşik analizinde, Spearman korelasyon katsayısı ve Spearman korelasyon katsayısı için p-değeri sırasıyla grup 1 için -
0.328 ve 0.094 iken grup 2 için -0.200 ve 0.800 idi. Bu eşik değer etkisinin olmadığı anlamına gelmektedir.
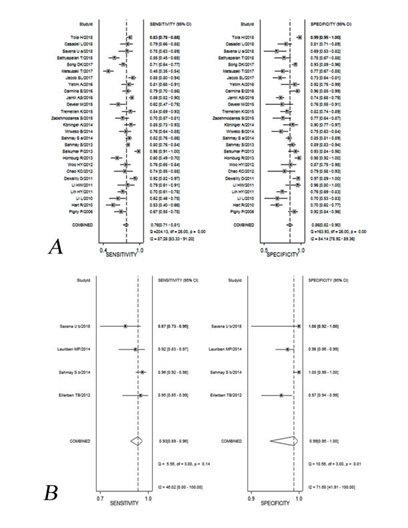
PKOS tanısında yalnız AMH testi için toplam sensitivite, spesifisite ve tanısal olasılık oranı sırasıyla 0.76 (%95 CI 0.71-
0.81), 0.86 (%95 CI 0.82-0.90) ve 20 (%95 CI 12-33). Toplam PLR ve NLR sırasıyla 5.5 (%95 CI 4.1-7.6) ve 0.28 (%95CI
0.22-0.34) idi. AMH’ın PKOM için alternatif tanı testi olarak kullanılması; toplam sensitivite, spesifisite ve tanısal olasılık
oranı sırasıyla 0.93 (%95 CI 0.89-0.96), 0.99 (%95 CI 0.95-1.00) ve 1634 (%95 CI 217-12324) idi (Figür 3). Toplam PLR
ve NLR sırasıyla 111.6 (%95 CI 18.7-666.1) ve 0.07 (%95 CI 0.04-0.11) idi.
PKOS için AMH’ın tek tanı testi olduğunda ve AMH PKOM yerine alternatif tanı testi olduğunda SROC eğrisi altındaki
alan (AUC) sırasıyla 0.88 (%95 CI 0.85-0.91) ve 0.97 (%95 CI 0.95-0.98) olarak ölçülmüştür ve bu oranlar anlamlı olarak
farklıdır (Z=4.89, P<0.01) (Figür 4).


TJODist
Bülteni

TJOD
İstanbul Şubesi
Meta regresyon ve subgrup analizi
Her ne kadar eşik etkisi olmasa da test sonuçlarındaki heterojenite başka faktörlerin etkili olduğunu göstermektedir.
Sensitivite ve spefisite için I-square; grup 1 için %87.26 ve %84.14 iken grup 2 için %46.02 ve %71.06 idi. Bu yüzden,
grup 1 için rasgele etki modeli geliştirilmiştir ve sonuçlar AMH için eşik değeri ve AMH kitinin sensitivite ve spesifisite
heterojenitesine neden olabileceğini göstermiştir.
TARTIŞMA
PKOS kadınlardaki anavulatuar infertilitenin %80’ini oluşturmaktadır. PKOS’lu hastalarda diabet gibi inatçı endokrin
hastalıklar daha sık görülmektedir. PKOS’un neden olabileceği problemler düşünüldüğünde erken tanı önemlidir.
Geleneksel tanısal metodlar; transabdominal yada vajinal ultrasonda PKOM görünümünün izlenmesi; kan testinde
biyokimyasal HA veya klinik HA (hirsutizm, akne ve diğer semptomlar) ve OA semptomlarının izlenmesidir. Ultrasonografik
tanı için yeterli ultrasonografik cihazlara ve bunları etkin kullanabilen operatörlere ihtiyaç vardır. Bu durumda PKOM’un
sübjektif değerlendirmesi kaçınılmaz olmaktadır. Ayrıca PKOM tanısındaki eşik folikül sayısında da fikibirliği yoktur. Tüm
bu faktörler tanısal sensitivite ve spesifisiteyi etkilemektedir. AMH folikül sayısı ile yakından ilişkilidir ve PKOS tanısından
daha iyi bir tanısal test olarak değerlendirilir. Konu ile ilgili birçok çalışmada sensitivite ve spesifisite farklılıkları vardır.
Iliodromiti ve ark.’nın konu ile ilgili meta-analizinde yalnızca 10 makale mevcuttur ve bu durum bias riskine neden olabilir.
Bu yüzden bu meta-analiz ile AMH’ın tek başına PKOS tanısındaki yeri ve Rotterdam kriterlerinde PKOM yerine
kullanılabilirliği değerlendirilmiştir.


TJODist
Bülteni

TJOD
İstanbul Şubesi
Bu meta-analizde; yalnız AMH’ın PKOS tanısında kullanılması ile sensitivite, spesifisite ve tanısal olasılık oranı (DOR)
sırasıyla 0.76 (95%CI 0.71-0.81), 0.86 (95%CI 0.82-0.90) ve 20 (95%CI 12-33) idi. AMH, PKOS tanısında Polikistik Over
Morfolojisi (PKOM) yerine kullanıldığında sensitivite, spesifisite ve tanısal olasılık oranı (DOR) sırasıyla 0.93(95%CI 0.89-
0.96), 0.99 (95%CI 0.95-1.00) ve 1634 (95%CI 217-12324) idi.
Düşük tanısal yeterlilik çalışmalardaki PKOS tiplerinin farklılığından kaynaklanmaktadır. Hastada PKOM bulgusu yok iken
HA ve OA ile seyreden PKOS tanısı varsa AMH’ın PKOS tanısında tanısal yeterliliği düşüktür. Bu yüzden subgrup analizi
yapılmaya çalışılmıştır fakat bilgi yetersizliğinden dolayı bu analiz yapılamamıştır.
Diğer subgrup analizlerinde anlamlı sonuçlara ulaşılmıştır. Beyaz ırkta yapılan subgrup analizinde sensitivite ve
spesifisitenin diğer ırklarla benzer sonuçlara sahip olduğu görülmüştür böylece ırk farketmeden AMH’ın tanıda
kullanılabileceği görülmüştür. BMI için keza kilo ile AMH değerleri açısından farklılık olmadığından AMH testi tüm
BMI’larda universal olarak kullanılabilir. Yaşa göre subgrup analizi yapılığında SEN, SPE ve AUC belirgin olarak ileri
yaşlarda daha yüksek olduğu görülmüştür, bu yüzden adölesanlarda AMH uygun bir tanısal test değildir. Bu meta-analizi
sonucuna bakıldığında AMH kiti ve AMH eşik değeri sensitivite ve spesifisite heterojenitesinin kaynağını oluşturur. Belirli
bir kitin diğerinden daha iyi olduğu söylenemez ve belirlenebilmiş bir eşşik değer maalesef yoktur.
AMH’ın geleneksel kan testlerinden farklı olarak adetin her döneminde bakılabilir olması kullanımını güçlendirir. Bazı
vajinal ultrason yapılamayan adölesanlarda AMH kullanımı faydalı olabilir. AMH; HA ve OA ile birleştirildiğinde PKOS’un
öngörüsünde klinik yeterlilik ile tanısal değeri güçlenir. Fakat hala AMH ile ilgili bazı problemlerin hızla çözülmeye ihtiyacı
vardır. Farklı AMH kitlerinin farklı tanısal yeterlilikleri vardır ve yaş-eşleşmeli AMH eşik değerinin PKOS hastaları ile PKOS
olmayan hastalar arasında ayrımı yapmadaki yeterliliği belirsizdir. Bu yüzden gelecek testlerin aynı AMH kiti ve eşik
değeri ile yapılması gerekmektedir.
Bu meta-analiz PKOS tanısında AMH’ın tanısal değerinin belirlenmesini ve güncellenmesini amaçlamıştır ve PKOM’un
alternatif tanısında AMH’ın yerinin belirlenmesini hedeflemiştir; fakat bu meta-analizin de bazı limitasyonları
bulunmaktadır. Öncelikle; sadece İngillizce literatür dahil edilmiştir bu seçim biasına neden olabilir; ikinci olarak, tanısal
kriteri değiştirmemek adına sadece 2003 Rotterdam kriterlerinin kullanıldığı çalışmalar eklenmiştir, bu da seçim biasına
neden olabilir; üçüncü olarak çalışmaların çoğunluğunu retrospektif çalışmalar oluşturmaktadır ; seçim biasını engellemek
ve istatistiksel güvenirliği artırmak adına daha çok prospektif çalışma dahil edilmelidir; dördüncü olarak PKOM tanısında
AMH kullanımı araştıran çalışma sayısı yalnızca dört tanedir ve spesifisite heterojenitesi açıklanamaz.
Sonuç olarak; Bu güncel meta-analiz AMH’ın PKOS tanısında potansiyel biyomarker özelliğini ortaya koymuştur ve
PKOM tanısında AMH’ın alternatif klinik değerini göstermiştir. Fakat adölesan kızlarda AMH’ın kullanımı hala tartışmalıdır,
klinik uygulamaya geçirilmesi hemen olmayabilir. Daha çok prospektif çalışma ile AMH eşik değeri belirlenmelidir.


TJODist
Bülteni

TJOD
İstanbul Şubesi
Anti-Müllerian
hormon
(AMH)
seviyeleri
dünya
genelinde
kadın
fertilite
süresini
tarama
aracı
olarak
kullanılmaktadır.
Her
ne
kadar
AMH
düzeyleri
menopoz
yaşıyla
ilişkili
olsa
da,
tek
bir
AMH
ölçümü
ile
menopoz öngörüsü güvenilir değildir.
Amaç:
Bu
çalışmada,
AMH’daki
düşüş
paternlerinin,
tek
bir
ölçümle
karşılaştırıldığında
menopoz
tahminini
iyileştirip
iyileştiremeyeceği araştırıldı.
Metod:
Çalışma
popülasyonu,
Doetinchem
kohort
çalışmasından
2.434
premenopozal
kadını
içermektedir.
Katılımcılar
toplam
20
yıl
boyunca
5
yılda
bir
takip
edildi
ve
picoAMH
testi
ile
6.699
plazma
örneğinde
AMH
ölçüldü.
Kadın
başına
seri
AMH
ölçümlerini
birleştirmek
için
zamana
göre
değişen
Cox
modellemesi
ile
longitudinal istatistik modelleme birleştirildi.
Bulgular:
Ortalama
menopoz
yaşı
50
idi
ve
izlem
sırasında
menopoza
giren
kadınların
%
7.4'ü
45
yaşından
önce
menopoza
girmişti.
25
yaşında
bir
kadın
için,
20-25
yaşları
arasındaki
AMH
düşüş
oranı
menopoz
öngörüsünde
C-istatistiği
0.64’ten
0.69’a
çıkarmıştır.
20
yaşın
üstünde,
AMH
düşüş
oranı
menopoz
veya
erken
menopoz
öngörüsünü
iyileştirmemiştir.
Menopoz
tahmininin
muhtemelen
en
önemli
olduğu
30
yaş
altı
kadınlar için, modeller erken menopoz riskini az hesaplamıştır.
Sonuç:
Bu
sonuçlar
AMH
düşüş
hızı
bilgisinin
menopoz
öngörüsünü
iyileştirmediğini
göstermektedir.
Erken
menopoz
riskini
öngörememesine
bağlı
olarak,
menopozun
zamanlaması
için
bir
tarama
yöntemi
olarak
AMH
kullanımı
şu anda savunulmamaktadır.
Giriş
AMH
kadınlar
arasında
farklı
bir
hızda
azaldığı
için,
seri
AMH
ölçümlerinin
kullanılmasıyla
AMH'nın
bireysel
düşüş
oranı
dikkate
alınarak
menopoz
öngörüsü
potansiyel
olarak
iyileştirilebilir.
Bugüne
kadar,
bir
çalışmada
menopoza
girişte
seri
AMH
ölçümleri
araştırılmış,
ancak
seri
AMH
ölçümleri
ile
tek
bir
ölçüm
karşılaştırılmamıştır.
Bu
nedenle,
bu
çalışmanın
amacı,
bireysel
AMH
düşüşünün,
genel
popülasyondaki
menopozun, özellikle erken menopozun öngörüsünü iyileştirip iyileştiremeyeceğini araştırmaktır.
Metod
Bu
çalışma
için,
Doetinchem
kohort
çalışmasının
kadın
katılımcılarından
elde
edilen
veriler
kullanıldı.
Doetinchem
kohort
çalışması,
1987
yılında,
Hollanda'daki
Doetinchem
kasabasında
yaş
ve
cinsiyete
dayalı
3.641
erkek
ve
4.128
kadın
nüfustan
oluşan
rastgele
örneklemle
ortaya
çıkmıştır.
Başlangıç
vizitinden
sonra
katılımcılar
her
5
yılda
bir
izleme
davet
edildi.
Her
ziyarette
bir
anket,
antropometrik
ölçümler
ve
açlık
kan
örneği
alındı
(ancak
bunlarla
sınırlı
değildi).
Plazma
örnekleri,
ileride
kullanılmak
üzere
saklandı.
Bu
çalışma
sırasında,
5
ziyaret
tamamlandı
ve
yaklaşık
20
yıllık
bir
takip
süresine
ulaşıldı.
Çalışmadaki
premenopozal
kadınlar çalışma popülasyonuna dahil edildi. Toplam 2.434 kadın çalışmaya dahil edildi.


TJODist
Bülteni
ÇOK SAYIDA AMH ÖLÇÜMÜYLE MENOPOZ ÖNGÖRÜSÜ İYİLEŞTİRİLEBİLİR Mİ?
PROSPEKTİF DOETİNCHEM KOHORT ÇALIŞMASININ SONUÇLARI
Can menopause prediction be improved with multiple AMH measurements? Results from the prospective
Doetinchem Cohort Study de Kat AC, van der Schouw YT, Eijkemans MJC, Broer SL, Verschuren WMM, Broekmans
FJM. Can Menopause Prediction Be Improved With Multiple AMH Measurements? Results From the Prospective
Doetinchem Cohort Study. J Clin Endocrinol Metab. 2019 Nov 1;104(11):5024-5031. doi: 10.1210/jc.2018-02607.
PubMed PMID: 31006802.
Özetleyen: Dr. Berna Aslan Çetin


TJOD
İstanbul Şubesi


TJODist
Bülteni
Anketlerin
kullanımıyla
son
adet
dönemi
sırasındaki
yaş
değerlendirildi.
Anketlerde
mevcut
ve
önceki
menstruasyon
durumu,
son
adet
dönemi
tarihi,
önceki
12
aydaki
adet
dönemlerinin
sayısı,
hormonal
kontrasepsiyon
kullanımı
hakkında
bilgiler
içermektedir.
Menopoz
durumu
ve
son
adet
döneminin
zamanlaması her bir turda değerlendirildi.
Menopoz
ve
erken
menopoz
tahmini
için
bir
tahmin
modeli
geliştirmek
amacıyla,
bir
bireyde
zaman
içinde
seri
AMH
ölçümlerinden
faydalanmak
için
zamanla
değişen
değişkenlere
sahip
Cox
hazard
modelleri
oluşturulmuştur.
Her
birey
için
tahmini
AMH
seviyelerini
türetmek
için,
her
bir
kadının
AMH
değişikliklerini
karakterize
etmek
için
tüm
çalışma
yaşı
aralığı
boyunca
logAMH
seviyesinin
(oral
kontraseptif
kullanımına
ve
sigara
içme
durumuna
bağlı
olarak)
tahminini
veren
bir
doğrusal
etki
modeli
kullanılmıştır.
Tahmini
AMH
düşüş
oranı,
oral
kontraseptif
kullanımını
durdurmak
veya
sigara
içme
alışkanlıklarını
değiştirmek
gibi
yaşam
tarzındaki
son
değişiklikleri
tamamen
yansıtmadığından
emin
olmak
için
elde
edildi.
Ortaya
çıkan
model,
takip
aralığında
herhangi
bir
yaş
aralığı
için
AMH
seviyesinin
öngörülen
kapasitesini
ve
düşüş
oranını
sağlamaktadır.
Bu
faktörlerin
yokluğunun
farklı
bir
bulguya
yol
açıp
açmayacağına
karar
vermek
için
kan
alımı
sırasında sigara içmeyen ya da oral kontraseptif kullanmayan kadınlarla sınırlı bir duyarlılık analizi yapıldı.
Bulgular
Her
vizitte
sigara
içimi
ve
oral
kontraseptif
kullanımı
dikkate
alınarak,
AMH
seviyesindeki
her
birim
ng/mL
düşüş,
aynı
takip
aralığında
%23
(%
95
CI%
20
-%
26)
daha
yüksek
menopoz
riski
ile
ilişkilendirildi.
Erken
menopozla
ilişkili
olarak
AMH'nın
hazard
oranı
1.53'tür.
Birbirinden
bağımsız
olarak
dahil
edildiğinde,
spesifik
AMH
düzeyi
ve
düşüş
oranı,
menopoz
oluşumunun
önemli
belirleyicileriydi.
Hem
AMH
seviyesi
hem
de
düşüş
oranı
modele
dahil
edildiğinde,
sadece
AMH
seviyesi
anlamlı
bir
öngörücü
olarak
kaldı
(HR
1.22,
%
95
CI
1.16-1.28).
AMH
seviyeli
modelin
C
istatistiği,
AMH
düşüş
oranının
eklenmesinden
sonra
aynı
kalmıştır
(0,70,
%
95
CI
0,68-0,72).
Her
ziyarette
düşüş
oranının
veya
düşüş
oranı*yaş
etkileşiminin
eklenmesi,
menopozun
veya
erken
menopozun
öngörülmesi
için
C
istatistiklerini
geliştirmedi.
Sigara
içmeyen
ya
da
oral
kontraseptif
kullanıcısı
olmayan
1.526
kadından
elde
edilen
verilerin
kullanıldığı
duyarlılık
analizi
sonuçlarımızı
değiştirmedi.
25
yaşın
üstünde,
tüm
tahmin
modellerinin
performansı
tek
veya
çoklu
AMH
ölçümleri
için
benzerdi.
25
ve
30
yaşlarında
ölçülen
AMH
ile
erken
menopozu
öngören
model,
klinik
olarak
en
yüksek
ilişkiye
sahip
model
olarak
kabul
edildi.
Bu
modelin
kalibrasyonu,
çoğu
durumda,
erken
menopozun
gerçek
(gözlenen)
riskinin,
öngörülen
(beklenen)
riskten
daha
yüksek
olduğunu,
yani
modelin,
erken
menopoz
riskini
hafife
aldığını göstermiştir.
Tartışma
Tek
bir
AMH
ölçümü
kullanarak
menopoz
öngörüsünün
sınırlılıkları
göz
önüne
alındığında,
AMH
düşüşünün
değerlendirilmesinin
menopoz
öngörüsünde
iyileşmeye
yol
açabileceği
umulmuştur.
Aksine,
bu
çalışmada
AMH
düşüş
oranının
menopoz
ve
erken
menopoz
öngörüsünü
iyileştirmediği
bulunmuştur.
25
yaşının
üzerinde,
iki
AMH
ölçümü,
menopoz
oluşumunun
öngörülmesi
için
tek
bir
AMH
ölçümünden
daha
üstün
değildir.
AMH
düzeyleri
ile
menopoz
ilişkisinin
daha
önce
yaşla
orantılı
olmadığı
bulundu
ve
bu
da
AMH'nın
artan
yaşla
birlikte
menopozun
daha
zayıf
bir
öngörücüsü
olmasına
yol
açtı.
Sonuç
olarak,
bulgularımız
mevcut
verilerle
uyumlu
görünmektedir,
bu
da
menopoz
tahmininin
uzun
aralıklarla
seri
AMH
ölçümleriyle
daha
iyi
öngörülemeyeceği
anlamına
gelir.
Mevcut
çalışmanın
tartışılması
gereken
bazı
güçlü
yönleri
ve
kısıtlılıkları
vardır.
Güçlü
yönleri
arasında
nüfus
temelli
katılımcı
seçimi
bulunur
ve
sonuçların
genel
nüfusun
kadınlarına
genelleştirilmesi
sağlanır.
20
yıllık
bir
takip
döneminde
5
kez
ziyaret
edilen
tasarım,
menopoz
tahmininde
AMH
düşüş
hızı
ve
uzun
süreli
yaşın
çıkarımı
için
çok
uygundur.
Bu
çalışma,
menopoz
yaşı
ile
ilişkili
olarak
AMH
değişikliklerini
incelemek
için
bugüne
kadar
yapılan
en
büyük
çalışmadır
ve
çalışma
boyutunun
önemli
bir
avantajı, menopoz yaşı olan 96 kadının 45 yaşından önce menopoza girmesidir.

TJOD
İstanbul Şubesi


TJODist
Bülteni
Bu
çalışmanın
olası
bir
kısıtlılığı,
iki
vizit
ve
AMH
ölçümü
arasındaki
5
yıllık
sürenin
menopozla
ilgili
gelecekteki
durumunu
öğrenmek
isteyen
birisi
için
uzun
olmasıdır.
AMH'nın
30
yaşından
sonra
kısa
süreli
periyotlarda
ve
menstruel
siklus
boyunca
sabit
kaldığı
veya
0,5
ng
/
mL'ye
kadar
değiştiği
düşünülmektedir.
Doetinchem
kohort
çalışmasında
her
bir
takip
aşamasındaki
yaş
dağılımı
normaldi;
böylece,
AMH
ölçümleri
tüm
yaş
aralığında mevcuttu.
Bir
başka
kısıtlılık
ta,
menopoz
yaşının
tamamen
anketlerle
değerlendirilmesi
ve
dolayısıyla
hatırlama
biasına
neden
olmasıdır.
Menopoz
ile
anket
arasındaki
zaman
farkı
en
fazla
5
yıl
olduğundan
ve
herhangi
bir
tutarsızlık,
çoklu
anketler
kullanılarak
filtrelendiğinden,
menopozda
yaşın
yanlış
sınıflandırılmasının
sonuçlarımıza büyük bir etkisinin olacağını düşünmüyoruz.
Son
olarak,
menopozun
öngörülmesi,
sonuçta
kadınların
ilgisi
olan
doğurganlık
süresinin
öngörülmesine
karşılık
gelmez.
Yakın
zamandaki
prospektif
bir
çalışmada
30-44
yaşları
arasındaki
kadınlarda
AMH
düzeyleri
ile
gebeliğe
kadar
geçen
süre
ve
kümülatif
gebe
kalma
oranları
arasında
bir
ilişkisi
bulunamamıştır.
Doetinchem
kohort
çalışmasında
gebelikler
hakkındaki
veriler
takip
edilmediğinden,
AMH'nın
bu
kohorttaki
fertilite
sonuçları
ile
ilişkilendirilmesi
mümkün
değildi.
Duyarlılık
analizimize
dayanarak,
bu
kısıtlılıkların
ana
sonuçlarımızı etkilemediği görülüyor.
Sonuç
olarak,
zaman
içerisinde
seri
AMH
seviyelerinin
ölçümü,
tek
bir
AMH
ölçümüyle
karşılaştırıldığında,
menopoz
oluşumunda
bireysel
risk
öngörüsünü
iyileştirmez.
Sonuçlarımız,
aile
planlaması
konusunda
tavsiye
isteyen
kadınların
AMH
düzeylerini
tek
veya
seri
olarak
taramaktan
faydalanmasının
mümkün
olmadığını
düşündürmektedir.

TJOD
İstanbul Şubesi
Özet:
Morselasyon
uterus
veya
miyomun
boyutunu
küçülterek
dokunun
küçük
kesilerden
veya
laparoskopik
aletlerle
çıkarılmasını
sağlamak
amacı
ile
kullanılan
cerrahi
bir
tekniktir.
Semptomatik
miyomlar
nedeni
ile
yapılan
histerektomi
ya
da
miyomektomi
operasyonları
sırasındaki
morselasyonun
beklenmedik
leiomiyosarkomun
yayılmasına
neden
olabileceği
bildirilmiştir.
Morselasyon
öncesi
hastalar
muhtemel
malignite
riskleri
açısından
değerlendirilmelidir.
Malignite
varlığında
morselasyon
kontrendikedir
ve
bu
nedenle
preoperatif
değerlendirme
önem
kazanmaktadır.
Ancak
leiomiyomların
preoperatif
tansındaki
güçlük
nedeni
ile
miyom
nedenli
yapılan
morselasyon
sonrası
malignitenin
yayılabileceği
ve
prognozu
olumsuz
etkileyebileceği
bilinmelidir.
Her
ne
kadar
açık
miyomektomi
ya
da
histerektomi
sırasında
leiomiyosarkom
yayılım
riskinin
daha
az
olabileceği
düşünülse
de,
minimal
invaziv
cerrahiler
ile
kıyaslandığında
cerrahi
ilişkili
morbidite
ve
mortalitenin
daha
yüksek
olduğu
bilinmektedir.
Morselasyona
ve
cerrahiye
bağlı
tüm
risklerin
alternatif
yöntemlerin
tartışıldığı
aydınlatılmış onam ile birlikte hem jinekologlar hem de hastalar karar sürecine ortak katılım sağlamalıdır.
Öneriler ve Sonuçlar
Amerikan
Kadın
Hastalıkları
ve
Doğum
Birliği
uterin
morselasyon
(manuel
ya
da
power
morselasyon)
ile
ilgili
aşağıdaki önerileri yapmaktadır
1
.
Açık
morselasyon
planlanan
hastalar
preoperatif
dönemde
uterin
malignensi
riski
açısından
değerlendirilmelidir.
2
.
Bu değerlendirme görüntüleme, servikal kanser taraması ve endometrial örneklemeyi içermelidir.
3
.
Hastalar,
açık
morselasyon
ile
tanı
konulmamış
malignensi
ya
da
benign
uterin
parçaların
yayılabileceği
konusunda bilgilendirilmelidir.
4
.
Her
ne
kadar
açık
histerektomi
ya
da
miyomektomi
tanı
konulmamış
leiyomiyosarkom
riskini
azaltsa
da,
minimal
invaziv
cerrahiler
ile
kıyaslandığında
cerrahi
ilişkili
morbidite
ve
mortalitenin
bu
operasyonlarda
daha yüksek olduğu bilinmektedir.
5
.
2017
Sağlık
Araştırmaları
ve
Kalite
Ajansının
(AHRQ)
raporuna
dayanarak
semptomatik
leiomiyom
ameliyatları
sonrası
leiomiyosarkom
riskinin
770
ameliyatta
1'den
az
ile
10,000'de
1
arasında
değiştiği
bilinmelidir.
6
.
Morselasyona
ve
cerrahiye
bağlı
tüm
risklerin
alternatif
yöntemlerin
tartışıldığı
aydınlatılmış
onam
ile
birlikte hem jinekologlar hem de hastalar karar sürecine ortak katılım sağlamalıdır.
Giriş
Morselasyon
uterusu
küçültmek
ya
da
miyomları
daha
küçük
parçalara
ayırarak
daha
küçük
insizyonlardan
çıkarabilmek
amacı
ile
on
yıllardır
jinekologlar
tarafından
kullanılan
bir
cerrahi
tekniktir.
1993
yılında
geliştirilmiş,
morselatör
olarak
bilinen
elektromekanik
aletler
dokuyu
kesme
ya
da
tıraşlama
amacı
ile
kullanılmaktadırlar.
Uterus
ya
da
miyomların
açık
morselasyonu,
olası
leiomiyosarkom
yayılma
riski
nedeni
ile
üzerinde
durulması
gereken
bir
konu
olmuştur.
Bu
nedenle,
Amerikan
İlaç
ve
Gıda
birimi,
2014
yılında,
fibroid
nedeni
ile
miyomektomi
yada
histerektomi
olan
kadınlarda
laparoskopik
morselatör
kullanımına
yönelik
bir
uyarı
yayımlamıştır.
Bu
bildiriden
sonra,
laparoskopik
miyomektomi
ve
histerektomi
oranları
önemli
ölçüde
azalmıştır.
Ancak
bu
durum
abdominal
cerrahiye
bağlı
major
ve
minör
komplikasyonların
insidansında
artmaya
neden
olmuştur.
Her
ne
kadar
Amerikan
İlaç
ve
Gıda
birimi
morselasyon
hakkındaki
endişelerini
bildirmiş
olmasına
rağmen,
histerektomi
ve
miyomektomi
sırasında
yapılan
tüm
morselasyon
tekniklerinin,
farkında


TJODist
Bülteni
LEIOMIYOM NEDENI ILE YAPILAN MORSELASYON
Uterine Morcellation for Presumed Leiomyomas
ACOG Committee Opinion No. 770. Obstet Gynecol. 2019 Mar;133(3):e238-e248.
Özetleyen: Dr. Cihan Kaya


TJOD
İstanbul Şubesi


TJODist
Bülteni
olunmayan kanser hücrelerini tüm pelvis ve abdomene yayma potansiyeline sahip olduğu bilinmelidir.
Bu
yazıdaki
ana
amaç
semptomatik
miyomların
cerrahisine
dikkat
çekmektir.
Morselasyondan
kasıt
ise,
spesmenin
peritoneal
kavite
içerisinde
herhangi
bir
koruyucu
torba
içine
alınmadan
çıkarıldığı
açık
morselasyondur. Bu bilgiler histeroskopik miyomektomi için geçerli değildir.
Epidemiyoloji
Uterin
leiomiyomlar
sık
görülmelerine
rağmen,
leiomiyosarkom
insidansı
100.000
kadın-yaşta
0.36
olup,
leiomiyosarkomun
görüldüğü
median
yaş
54’tür.
Leiomiyosarkomun
pelvik
radyasyon
hikayesi
ve
herediter
retinoblastoma
ya
da
Li
Fraumeni
gibi
bazı
herediter
kanser
sendromları
ile
ilişkili
olduğu,
ancak
uterus
büyüklüğü ya da hızlı uterin büyüme ile ilişkili olmadığı gösterilmiştir.
Preoperatif Değerlendirme
Açık
morselasyon
düşünülmeden
önce
hastanın
uterin
malignensi
riskinin
olup
olmadığı
değerlendirilmelidir.
Bunun
için
uygun
görüntüleme,
servikal
kanser
taraması
ve
endometrial
doku
örneklemesi
yapılmalıdır.
Görüntülemede
şüpheli
bulgular,
patolojik
değerlendirme
yapılmamış
anormal
uterin
kanama
ya
da
tedavi
edilmemiş servikal lezyon varlığı, morselasyon yapılmamasını gerektirir.
Tüm
bunlarla
beraber
endometrial
örnekleme
dahil,
hiçbir
preoperatif
testin
leiomiyosarkomu
kesin
olarak
dışlayamayacağı
da
bilinmektedir.
Dinamik
manyetik
rezonans
görüntüleme
(MRI)
ve
laktat
dehidrojenazın
(LDH)
leiomiyosarkomların
preoperatif
değerlendirilmesinde
rolü
olabileceği
öne
sürülmüştür,
ancak
bu
verilerin
kanıt
düzeyi
zayıf
klinik
çalışmalar
ile
sınırlıdır.
Bunun
yanısıra,
leiomiyomlardan
biyopsi
alınması
tartışmalı
olup
bu
invaziv
girişimin
faydalı
olduğunu
destekleyen
çalışma
bulunmamaktadır.
Ayrıca
işlem
ile
ilişkili risklerin olması ve kar-zarar oranı gözetildiği zaman biyopsi seçeneği pratik görünmemektedir.
Leiomiyom Düşünülen Kadınlarda Leiomiyosarkom Riski
Miyomatö
uterusu
olan
kadınlardaki
leiomiyosarkom
riski
konusunda
henüz
net
bir
konsensus
sağlanmamıştır.
2014
yılında
FDA
tarafindan
yapılan
değerlendirmede
1980-2011
yılları
arasında
miyomları
nedeni
ile
histerektomi
ya
da
miyomektomi
olmuş
hastalar
değerlendirilmiş
ve
şüphelenilmeyen
uterin
sarkom
ile
leiomiyosarkom
prevalansı
ortaya
konmuştur.
Toplamda
9160
hastanın
dahil
olduğu
9
çalışmadan
oluşan
bu
analize
göre,
benign
leiomiyom
nedeni
ile
opere
olmuş
bu
hastaların
1/352’sinde
uterin
sarkom,
1/498’sinde
leiomiyosarkom
saptanmıştır.
Bu
çalışmada
leiomiyom
çıkmayan
hastalara
ait
çalışmaların
dışlanması
nedeni
ile
muhtemelen
verilen
prevelans
oranları
abartılmıştır.
Bu
analiz
FDA’in
Kasım
2014
Güvenlik
Rehberinde,
‘….uterus
şüpheli
doku
taşıyabilir
ve
laparoskopik
power
morselatör
kullanımı
ile
bu
hücrelerin
yayılması
artarak
uzun
dönem
hasta
sağkalımını
azaltabilir.
Bu
bilgiler
hastalar
ile
de
tartışılmalıdır’şeklinde
yerini
almıştır.
Ayrıca
aynı
sayıda
‘’…laparoskopik
power
morselerasyonun
şüpheli
fibroidler
içeren
uterusu
olan
peri-
post
menapozal
hastalarda
kontrendike
olmasının
bilinmesi
veya
bu
hastalarda
enblok
spesmenin
çıkarılması…’’ gerekliliğini bildirmişlerdir.
2017’de
FDA,
son
3
yılda
konu
ile
ilgili
yapılan
23
çalışmanın
analizini
yapmış
ve
tahmin
edilen
sarkom
prevelansı
1/305-1/360
arasında
ve
leiomiyosarkom
oranı
1/570
ile
1/750
arasında
çıkmıştır.
Bu
değerler
önceki
analiz
ile
uyumlu
olduğundan,
FDA
güvenlik
rehberindeki
morselatörlere
yönelik
uyarılara
devam
etmiştir.
Diğer
çalışmalar
miyom
nedeni
ile
yapılan
cerrahiler
sonrası
leiomiyosarkom
riskinin
daha
düşük
olduğunu
göstermiştir.
2015
yılında
yapılmış
olan
133
çalışmanın
dahil
edildiği
bir
meta-analizde
leiomiyosarkom
riskinin
1961’
de
1
(%0.051;
%95
güven
aralığı,
0.16-0.98)
olduğunu
bildirilmiştir.
Aynı
meta-analizdeki
sadece
64
prospektif
çalışmaya
ait
veriler
değerlendirildiğinde
bu
riskin
8300’
de
1
(%
0.012;
%
95,
güven
aralığı,
0.01-
0.75) olduğu görülmüştür.

TJOD
İstanbul Şubesi
2017
yılında
AHRQ
tarafından
yayımlanan
bir
sistematik
derlemede
160
çalışmadaki
136.195
hastaya
ait
veriler
incelenmiş
ve
datanın
%29’unu
prospektif
çalışmalar
oluşturmuştur.
Bu
meta-analize
göre
prospektif
çalışmalarda
genel
miyom
sonrası
leiomiyosarkom
riski
%0.02
(dağılım:%
0.05-0.09)
olarak
bildirilirken,
retrospektif
çalışmalarda
%0.08
(dağılım:
%0.05-0.13)
olarak
bildirilmiştir.
Cerrahi
başına
risk
hesaplandığı
zaman beklenmeyen leiomiyosarkom riskinin 10.000 de 1-13’ten az (1/10,000 ile 1/770) olduğu görülmüştür.
Leiomiyosarkomu Olan Hastalarda Morselasyonun Prognoza Etkisi
Leiomiyosarkom
intraperitoneal
ve
hematojen
yollar
ile
hızlıca
yayılan
agresif
bir
tümördür.
Ulusal
kanser
enstitüsü’nün
1998-2013
yılları
arasındaki
verilerine
göre
uterusa
sınırlı
(Evre
1)
tümörün
5
yıllık
sağkalım
oranı
%55.4’tür.
Leiomiyosarkom’un
morselasyonunun
hasta
prognozunu
kötü
etkilediği
ile
ilgili
kanıtlar
sınırlıdır.
Küçük
retrospektif
çalışmalar
morselatör
kullanılmış
hastalarda
leiomiyosarkom
rekürrensinde
ve
evresinde
artma
saptamışlardır.
Ancak
çalışmalar
arasındaki
heterojenite,
çalışmaların
retrospektif
oluşu
ya
da
çalışmaların az sayıda hasta ile yapılması bu ikilem ile ilgili kesin bir sonuca varılmasını engellemektedir.
Leiomiyosarkomlu
715
kadının
katıldığı
28
çalışmadaki
384
morselerasyonun
kullanıldığı
hastayı
içeren
24
çalışmanın
dahil
edildiği
2017
AHRQ
meta-analizi,
morselasyonun
etkisine
yönelik
önemli
katkılarda
bulunmuş
bir
çalışmadır.
Bu
çalışmada
sağkalım
aralıkları,
Bayesian
güven
aralığı
(BCI)
ile
ifade
edilmiştir.
Çalışmaya
göre
sağkalım
süresi
morselasyon
tekniğine
göre
değişmiştir.
5
yıllık
sağ
kalım
süresi,
power
morselasyon
tekniği
ile
%30
(%95
BCI,
%13–%61),
bistüri
ile
morselasyonda
%59
(%95
BCI,
%33–%84)
ve
hiç
morselasyon
yapılmayan
hastalarda
%60
(95%
BCI,
24%–98%)
oranında
bildirilmiştir.
Power
morselatör
ile
sağkalım
oranı
diğer
2
gruba
göre
anlamlı
derecede
düşük
olmasına
rağmen,
3
grubun
BCI
değerlerinin
örtüşmesi, özellikle uzun süreli takiplerde tahmin değerlerinin kesinlik oranını düşürmektedir.
Morselasyona Alternatif Yöntemler
Amerikan
Kadın
Hastalıkları
ve
Doğum
Birliği,
benign
nedenler
ile
histerektomi
olan
hastalarda
minimal
invaziv
yaklaşımı
önermektedir.
Uterusun
vajenden
intakt
çıkarmak
için
fazla
büyük
olduğu
durumlarda,
vajinal
histerektomiyi
tamamlayabilmek
için
morselasyon
gerekmektedir.
Bunun
alternatifi
abdominal
insizyon
ile
uterusu
çıkarmal
olabillir.
Benzer
şekilde
morselasyon
yapmadan
miyomektomi
yapmak
da
abdominal
insizyon
gerektirir.
Abdominal
yaklaşımda
da
power
morselasyonun
risklerinden
kaçınmak
amacı
ile,
bir
torba
içine
alarak
çıkarma,
ya
da
mini-laparatomi
ile
morselasyon
ya
da
vajinal
manuel
morselasyon
yapılabilir.
Morselasyonun
intraperitoneal
yayılımı
azaltması
ve
doku
çıkarılmasını
kolaylaştırmak
amacı
ile
birçok
farklı
koruyucu
torba
üretilmiştir.
Ancak
şimdiye
kadar
koruyucu
torba
içinde
spesmenin
çıkarılmasının
etkinliği
ile
ilgili
yeterli
çalışma
bulunmamaktadır.
Torbanın
sızdırmazlığı
hakkında
şüpheler
olduğu
gibi
torbanın
morselasyonu
zorlaştırarak
operasyon
süresini
uzatabileceğine
yönelik
endişeler
de
mevcuttur.
Torba
nedeni
ile
diğer
abdominal
organların
görülmesindeki
kısıtlanma
ve
buna
bağlı
potansiyel
yaralanmalar
da
bir
başka
sorundur.
Bu
nedenle
dokunun
ya
da
kanserin
peritoneal
kavite
içine
dağılmasını
engellemek
amacı
ile
yeni
yöntemlerin geliştirilmesine ihtiyaç vardır.
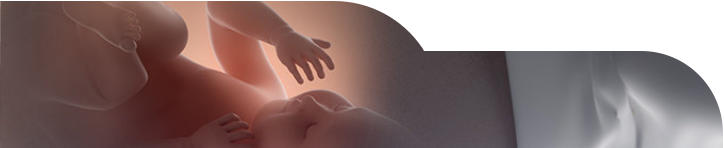
Laparoskopik ya da Abdominal Yaklaşım ile Yapılan Histerektomi ya da Miyomektomide Riskler
Şüphe
edilmeyen
malignitenin
yayılmasından
başka,
prosedürün
kendisinden
kaynaklı
morbiditeler
de
dikkate
alınması
gereken
durumlardır.
Abdominal
histerektomiler,
laparoskopi-asiste
vajinal
histerektomi
ya
da
laparoskopik
histerektomiye
göre
daha
fazla
enfeksiyon,
kanama,
venöz
tromboembolik
komplikasyonlar,
sinir
yaralanması,
genitoüriner
ve
gastrointestinal
yaralanmalar
gibi
olumsuz
sonuçlarla
ilişkili
olabilmektedir.
Abdominal
miyomektomi
de
benzer
risklere
sahiptir.
2014’te
yapılan,
808
hastayı
içeren
9
çalışmanın
dahil
edildiği
bir
meta-analize
göre,
laparoskopik
miyomektomi
abdominal
miyomektomiye
kıyasla
daha
az
postoperatif ağrı, ateş ve daha kısa hospitalizasyon süresi ile birlikte bulunmuştur.
Abdominal
histerektomi
ya
da
miyomektomi
teşhis
edilmemiş
leiomiyosarkomun
yayılma
riskini
azaltsa
da
minimal
invaziv
yaklaşıma
göre
artmış
morbidite
ile
ilişkilidir.
Bu
faktörler,
operasyon
sırasında
leiomiyosarkom
gelişmesi
riski
ile
kıyaslanmalıdır.
Bu
durum
leiomiyosarkomun
nadir
görülen
bir
tümör
olması
nedeni
ile
hastaya
farklı
cerrahi
yöntemlerin
risklerini
ve
yararlarını
anlatmayı
zorlaştırmaktadır.
Yani
bir
hastaya
leiomiyosarkom riskinin 1/498 ile 1/10000’den az gibi geniş bir aralıkta olabileceğini söylemek güç olabilir.


TJODist
Bülteni

TJOD
İstanbul Şubesi
Sonuçların
anlaşılabilirliğini
kolaylaştırmak
amacı
ile
genel
riskler
abdominal
ya
da
laparoskopik
histerektomi
gibi
işleme
bağlı
riskler
ve
morselasyona
bağlı
riskler
olmak
üzere
ikiye
ayırılarak
modelleme
çalışmaları
yapılmıştır.
Bir
çalışmada
abdominal,
morselerasyon
olmadan
laparoskopik
ve
power
morselerasyonla
birlikte
laparoskopik
histerektomi
simülasyon
modelleri
oluşturulmuştur.
Bu
modelde
genel
malignite
riski
%0.27
(1/370)
olarak
tahmin
edilmiştir.
Bu
modelde
bulunan
riskin
yaşa
bağlı
olarak
değişmekte
olduğu
bildirilmiştir.
Ayrıca
morselasyon
ile
birlikte
laparoskopinin
daha
az
yaşam
yılı
ile
birlikte
olduğu
görülmüştür.
Ancak
abdominal
prosedür
ile
kıyaslandığı
zaman
her
iki
laparoskopik
prosedürün
daha
iyi
sonuçlarla
birlikte
olduğu
bildirilmiştir.
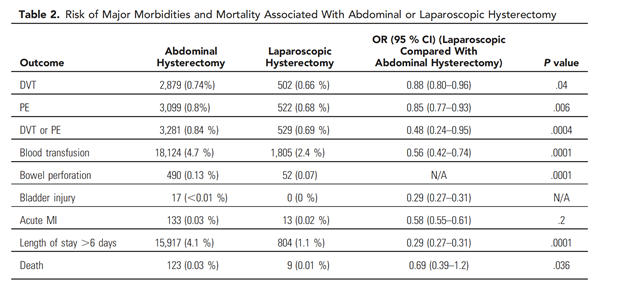
Yaşa
göre
alt
gruplara
ayırıldığı
zaman,
40
yaş
altında
laparoskopik
morselasyon
grubunda
10.000
de
0.94,
abdominal
histerektomi
grubunda
10.000
de
0.97
ölüm
olabileceği
gösterilmiştir.
Ancak
özellikle
60
yaş
ve
üstü
laparoskopik
morselasyon
grubunda
bu
oranlara
ek
olarak
10.000
de
18
daha
fazla
ölüm görüldüğü bildirilmiştir.
Ortak
karar
alma
modeline
dayalı,
10
bini
abdominal,
10
bini
laparoskopik
histerektomi
olmuş
toplam
20
bin
hastayı
kapsayan
bir
analize
göre,
abdominal
histerektomide
cerrahi
ile
ilişkili
morbiditenin
daha
fazla,
hospitalizasyonun
daha
uzun,
morselasyon
yapılan
laparoskopiye
göre
(leiomiyosarkom
riski
de
hesaba
katılarak)
daha
az
hasta
memnuniyetine
neden
olduğu
ortaya
konulmuştur.
Ancak
morselasyon
yapılan
laparoskopik histerektomi grubunda rekürrens görülme süresi ve genel sağ kalım daha az bulunmuştur.
2015
yılında
yayımlanan
ve
2017’de
güncellenen
karar
ağacı
modelini
kullanan
2
çalışma
FDA’nın
2014
uyarısından
sonra
yapılan
çalışmalara
ait
leiomiyosarkom
verilerini
kullanarak,
abdominal
ve
laparoskopik
histerektomi
olgularını
karşılaştırmıştır.
Ancak
bu
modelde
sensitivitenin
leimyoma
olduğu
düşünülüp
operasyon
sonrasında
leiomiyosarkom
olduğu
anlaşılan
kitle
prevalansı
ile
yüksek
oranda
ilişkili
olduğu
dikkate
alınmalıdır.
Örneğin
bu
çalışmalardan
2015’te
yapılanında,
kanser
ilişkili
mortalite
ile
prosedür
ilişkili
mortalite
oranı
bahsedilen
tahmini
leiomiyosarkom
prevelansına
bağlı
olup,
düşük
tahmini
prevelans
değerlerinde
laparoskopik
yaklaşım,
yüksek
tahmini
prevelans
değerlerinde
ise
abdominal
yaklaşım
avantajlı
bulunmuştur.
Tahmini
leiomiyosarkom
insidansı
0.0015
(1/667
ya
da
10000’de
15)
alındığı
zaman
iki
grup
arasındaki mortalite benzer bulunmuştur.
2017’de
yapılan
analizde
ise
yeni
çalışmaların
büyük
bir
kısmı
ele
alınarak,
leiomyosarkom
insidansı
(0.0017%
ya
da
1/558)
tahmin
edilmeye
çalışılmıştır.
Cerrahiye
bağlı
leiomiyosarkom
ve
mortalite
tahminleri
kullanılarak
yapılan
analizlerde
genel
mortalite
oranlarının
benzer
olduğu
görülmüştür.
Bu
çalışma
aynı
zamanda
yaşa
spesifik
leimiyosarkom
prevelansını
da
ortaya
koymayı
amaçlamıştır.
Hastalar
50
yaştan
genç
ve
yaşlı
olmak
üzere
ikiye
ayrılmış
ve
50
yaştan
genç
grupta
power
morselasyon
yapılan
laparoskopi
daha
avantajlı
bulunmuştur.
Laparoskopi
grubunda
leiomiyosarkoma
bağlı
16
daha
fazla
ölüm
saptanmış
iken,
laparoskopik
yaklaşımda
abdominal
yaklaşıma
kıyasla
20
daha
az
ölüm
görülmüştür.
Ancak
50
yaştan
daha
yaşlı
grupta
sonuçların
farklı
olduğu
bildirilmiştir.
Laparoskopik
histerektomi
grubunda
leiomiyosarkoma
bağlı
91
daha
fazla
ölüm
saptanmış
iken,
laparoskopik
yaklaşımda
abdominal
yaklaşıma
göre
70
daha
az
ölüm
görülmüştür.
Yazarlar
genel
mortalitenin,
laparoskopik
histerektomide
artmış
leiomiyosarkom
görülebilmesine
bağlı
ve
abdominal
histerektomide
artmış
prosedür
ilişkili
mortaliteye
bağlı
olarak
sonuçta
iki
grup
arasında
eşitlendiğini
bildirmişlerdir.
Bununla
beraber
yaşın
bir
risk
faktörü
olduğunu,
morselasyona
bağlı
ölüm
riskinin
50
yaş
üzeri
grupta daha yüksek olduğunu göstermişlerdir.
Bahsedilen
simülasyon
modelleri
ve
karar-ağacı
analizleri
riskleri
belirlemede
faydalı
olsa
da
bu
oranlar
2017
AHRQ meta-analizindeki oranlardan yüksektir.
Morselasyonun Diğer Riskleri
Kasım
2014
FDA
Güvenlik
Bildirisinden
sonra
yayımlanan
çalışmalar
çoğunlukla,
miyom
olduğu
düşünülen
ve
uygunsuz
biçimde
morsele
edilen
leiomiyosarkomlar
hakkındadır.
Ancak,
morselasyon
küçük
uteruslarda
laparoskopi
asiste
supraservikal
histerektomi
(LASH)
yapılırken
ya
da
prolapsus
cerrahisinin
bir
parçası
olarak
histerektomi
yapılırken
kullanılabilir.
Endometrium
kanseri
de
morselasyon
örneklerinde
saptanabilmektedir.
Power
morselasyon
kullanılan
10731
LASH
vakasının
retrospektif
analizine
göre,
8
hastada
endometrial
kanser
bulunmuştur
(%0.07
ya
da
1429’da
1).
Bu
çalışmada
ortalama
65.58
aylık
izleme
süresinde
hiçbir


TJODist
Bülteni

TJOD
İstanbul Şubesi
endometrial
kanser
tekrarlamamıştır.
Benign
endikasyonlar
ile
power
morselasyon
yapılan
başka
serilerde
ise
endomerial
kanser
%0.2-0.4
(250
de
1
ya
da
502
de
1)
sıklığında
saptanmıştır.
Bu
nedenle
özellikle
anormal
uterin
kanaması
ya
da
postmenopozal
uterin
kanaması
olan
hastalar
endometrial
adenokarsinoma
açısından
mutlaka uygun preoperatif değerlendirmeden geçmelidirler.
Bununla
beraber,
morselasyonun
diğer
istenmeyen
önemli
etkisi
benign
dokuları
da
periton
içine
yayabilmesidir.
2016
yılında
yapılan
bir
çalışmaya
göre,
morselasyon
sonrasında
intraperitoneal
endometriozis
(%1.4), adenomiyozis (%0.57), parazitik leiomiyoma ve nadiren yaygın peritoneal leiomiyomatosis görülebilir.
Enerji Kullanmadan Yapılan Morselasyon ve Vajinal Ekstraksiyon Sırasında Morselasyon
Morselasyon
ile
ilgili
endişeler
öncelikli
olarak
power
morselasyon
ya
da
abdominal
kavite
içinde
yapılan
morselasyona
yönelik
olmuştur.
Bistüri
ile
morselasyon,
vajinal
histerektomi
ya
da
total
laparoskopik
histerektomide
büyük
uterusları
vajenden
çıkarırken
yapılabilmektedir.
Teorik
olarak
bu
durumlarda
da
henüz
teşhis
edilmemiş
malign
hücreler
yayılabilmektedir.
Ancak
konu
ile
ilgili
yeterli
veri
bulunmamaktadır.
Bu
nedenle
laparoskopik
histerektomi
sırasında
uterusun
vajenden
morsele
edilerek
çıkarılması
planlanmş
ise,
vajinal ekstraksiyondan önce uterus bir spesmen torbasının içine alınmalıdır.
Birlikte Karar Verme Süreci
Miyomların
cerrahi
tedavisinde
morselasyon
kullanılıp
kullanılmaması
ile
ilgili
olarak,
hasta
ve
doktor
beraber
karar
almalıdır.
Hastaya
işlemin
fayda
ve
zararları,
alternatifleri
hakkında
bilgi
verilmeli,
işlem
ile
ilgili
uygun
onam
alınmalıdır.
Hasta
açık
morselasyon
ile
benign
ya
da
malign
uterin
dokunun
karın
içine
yayılabileceğini
bilmelidir.
Güncel
kanıtlar,
leiomiyosarkom
riskinin
az
olduğunu
göstermektedir
ancak
prevalans
tahminleri
net
olmayıp
geniş
bir
aralıkta
bulunmakta
ve
bu
durum
hastanın
riskin
boyutunu
anlamasını
zorlaştırmaktadır.
Yine
de
hastalar,
şimdiye
kadar
yapılmış
en
geniş
kapsamlı
rapor
olan
2017
AHRQ
bildirisine
göre
miyomlardan
beklenmeyen
bir
leiomiyosarkom
çıkabilme
ihtimalinin
1/770
ile
1/10.000
aralığında
değişebileceğini
bilmelidirler.
Benzer
şekilde,
hastalar
operasyon
tipinin
morbidite
ve
mortaliteyi
etkileyebileceğini
ancak
ameliyat tipinden bağımsız olarak leiomiyosarkomun kötü prognozu hakkında bilgi sahibi olmalıdırlar.
Bu
yaklaşımla,
hastaların
kendileri
de
laparoskopik
ya
da
laparotomik
yaklaşım
kararı
sürecinde
aktif
rol
oynamış
olacaklardır.
Yaşa
göre
sınıflandırılmış
model
çalışmalarına
göre,
yaşlı
grup
daha
yüksek
leiomiyosarkom
riski
taşımaktadır
ve
bunun
mortaliteye
etkisi
farklı
cerrahi
yaklaşımlar
ile
değişkenlik
göstermektedir.
Bununla
beraber,
yaşlı
gruptaki
hastaların
semptomatik
miyomlara
sahip
olması
ve
bu
nedenle
histerektomi
ya
da
miyomektomi
olması
sık
görülen
bir
durum
değildir.
Zaman
içerisinde
hasta
ve
doktor
arasındaki karşılıklı paylaşımlar, hastanın karar vermedeki otonomisini arttıracaktır.
Sonuç
Morselasyon,
uterusu
ya
da
miyomları
küçük
bir
insizyondan
çıkarabilmeyi
sağlayan
ve
minimal
invaziv
cerrahi
konsepti
ile
uyumlu
bir
yöntemdir.
Morselasyon,
vajinal,
laparoskopik
ya
da
abdominal
cerrahi
sırasında
ya
da
bistüri,
makas
veya
enerji
kullanılarak
yapılabilir.
Büyük
bir
uterus
için
morselasyona
alternatif
en
sık
kullanılan
yöntem
abdominal
histerektomidir.
Ancak
abdominal
histerektomi,
minimal
invaziv
yöntemlere
kıyasla
daha
fazla morbidite ve mortalite ile ilişkilidir.
Malign
bir
dokunun
morselasyonu
kontrendikedir
ve
bu
nedenle
kadınlar
preoperatif
kapsamlı
bir
malignensi
taramasından
geçmelidirler.
Ancak
leiomiyosarkomlar
preoperatif
dönemde
kesin
olarak
saptanamazlar.
Bu
nedenle
leiomiyom
sanılan
bir
fibroidin
morselasyon
ile
dağıtılan
bir
leiomiyosarkom
olma
riski
her
zaman
vardır.
Bu
risk
1/498’den
1/10.000’e
kadar
geniş
bir
skalada
olabilmektedir.
Bu
nedenle,
histerektomi
ya
da
miyomektomi
prosedürüne
bağlı
riskler
ile
öngörülemeyen
bir
malignitenin
riskleri
birbirini
dengelemelidir.
Şimdiye
kadar
bu
denge,
genç
hastalarda
minimal
invaziv
yaklaşımı
destekler
nitelikte
olup,
postmenopozal
hastalarda
(yapılan
çalışmalarda
50
yaş
kestirim
yaşı
olarak
kabul
edilmişitr)
ise
morselasyondan
kaçınılması
şeklinde
olmuştur.
Bu
noktada
jinekolog
ve
hasta,
ameliyat
tipinin
risk
ve
faydalarını
tartışmalı,
morselasyona
alternatif
yöntemler
açıklanmalı
ve
hasta-doktor
beraber
karar
vermelidir.
Sonuç
olarak,
leiomiyosarkom
risk


TJODist
Bülteni

TJOD
İstanbul Şubesi
faktörlerini
belirlemek,
leiomiyosarkomun
gerçek
prevalansını
hesaplayabilmek,
morselasyonun
güvenliğini
artırabilmek
amacı
ile
preoperatif
diagnostik
araçlar
ve
yöntemleri
geliştirebilmek
için
daha
çok
çalışmaya
ihtiyaç vardır.

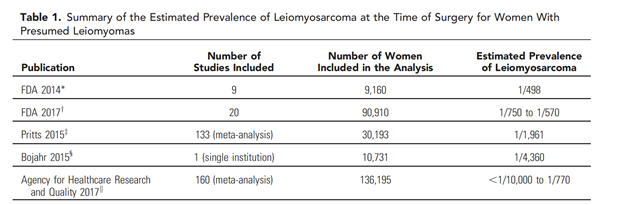


TJODist
Bülteni

TJOD
İstanbul Şubesi
Giriş
Kadınların
önleyici
hizmetler
girişiminin
(WPSI)
görevi
Birleşik
Devletler
önleyici
hizmetler
görev
gücünün
(USPSTF) sunduğu kılavuzlarda ki boşlukları doldurarak kadın sağlığını iyileştirmektir.
Meme kanseri
Kadınlarda
en
sık
görülen
kanserdir.
Son
bilgilere
göre
8
kadından
biri
yaşamı
süresince
meme
kanseri
teşhisi
alacaktır.
İnsidans
yıllık
%
0,4
oranında
artmaktadır.
Genel
olarak
mortalite
1989
yılında
tepe
noktasında
yüzbinde
33,2
iken
2016
yılında
%40
düşerek
yüz
binde
20
ölüme
düşmüştür.
Mortalitede
azalma
erken
tanıda
ki
iyileşmeler
meme
sağlığı
ile
ilgili
genel
farkındalığa
bağlı
olabilir.
Ortalama
meme
kanseri
riski
olan
kadınların
tarama
mamografisi
ile
40
-
50
yaş
arasında
başlanması
önerilmektedir.
Tarama
74
yaşına
kadar
devam etmeli yalnızca yaşın aramayı sonlandırma kriteri de olmamalıdır.
Tarama kılavuzları
Klinik meme muayenesi
Rutin
olarak
klinikte
uygulansa
da
anormal
bulgular
yüksek
yanlış
pozitif
oranlarına
sahiptir.
Bir
kanseri
yakalamak için 55 yanlış pozitif test yapılmaktadır.
Güncel
kılavuzlarda
Amerikan
kanser
cemiyeti
meme
muayenesi
önermektedir.
USPSTF
muayeneyi
ne
önermekte
ne
de
karşısındadır.
Amerikan
obstetri
ve
jinekoloji
cemiyeti
(ACOG)
25
ile
39
yaşları
arasında
1
ile
3
yıl
arasında
40
yaşından
sonra
ise
yıllık
meme
muayenesi
önermektedir.
Ulusal
kanser
ağı
(NCCN)
Amerikan obstetri ve jinekoloji ile aynı görüştedir.
Kadınların
kendi
meme
muayenesini
yapması
tartışmalı
bir
konudur.
Yüksek
yanlış
pozitifliğe
neden
olmaktadır.
Alternatif
olarak
kadınların
meme
farkındalığına
cesaretlendirilmesi
önerilmektedir.
Meme
yapısı
meme
akıntısı
drenaj
veya
yeni
kitle
oluşumu
gibi
değişiklikleri
hastanın
takip
etmesi
önerilmektedir.
Meme
farkındalığı ile kadınların yarısı meme kanserini belirleyebilmektedir.
Mamografik tarama
Amerikan
kanser
cemiyeti
40
yaşında
başlangıç
mamografisinin
yapılmasını
ve
45
yaşından
sonra
2
yılda
bir
tarama
ve
55
yaşından
sonra
yıllık
tarama
yapılmasını
önermektedir.
Beklenen
yaşam
süresi
10
yıldan
kısa
ise tarama kesilebilir.
USPSTF
ise
mamografik
taramanın
50
yaşından
sonra
başlanmasını
önermektedir.
40-49
yaş
arası
tarama
hasta
ile
kar
ve
zarar
açısından
tartışılması
gerektiğini
belirtilmektedir.
Yıllık
tarama
önerilmektedir.
Hangi
yaşta taramanın sonlandır alacağı ile ilgili yeterli kanıt bulunmadığını belirtilmektedir.
ACOG
40
yaşında
mamografik
taramanın
başlatılmasını
önermektedir.
Yıllık
veya
2
yılda
bir
olarak
75
yaşına
kadar devam edilmesini önermektedir.
NCCN
40
yaşında
başlanarak
yıllık
tarama
ve
yaşam
süresi
10
yılın
altında
olduğunda
taramanın
kesilmesini
önermektedir.


TJODist
Bülteni
KADINLARDA KANSER TARAMASI
Cancer Screening in Women.
Vogell A, Evans ML. Obstet Gynecol Clin North Am. 2019 Sep;46(3):485-499.
Özetleyen: Dr. Engin Çelik


TJOD
İstanbul Şubesi


TJODist
Bülteni
Erken
taramaya
başlama
ve
sık
taramanın
avantaj
ve
dezavantajları
bulunmaktadır.
Tarama
ile
hastalık
erken
teşhis
olurken
gereksiz
invazif
testlere
neden
olmaktadır.
Meme
kanser
tarama
konsorsiyumun
yaptığı
bir
derlemede
10
yıllık
kümülatif
yanlış
pozitif
oran
2
yıllık
taramada
%42
iken
yıllık
taramada
bu
oran
%61’e
yükselmektedir.
USPSTF
40
yaşından
başlayarak
yıllık
tarama
ile
kansere
bağlı
ölüm
de
bir
azalma
(8
vs
7),
yüksek
yanlış
pozitif
oran,
yüksek
gereksiz
meme
biyopsisi
ve
21
vs
19
yanlış
tanı
almış
meme
kanserine
neden olmaktadır.
Taramanın
arttırılması
radyasyona
maruziyeti
de
arttırmaktadır.
40
yaşından
başlayarak
yıllık
tarama
yapılması
ile
yüzbinde
11
radyasyona
bağlı
kanser
görülürken
50-59
yaşlarında
başlayan
2
yıllık
taramada
bu
oran
yüzbinde 2 olarak görülmektedir.
Özel popülasyonlar
Bazı
kadınlar
önceki
tedavi
veya
meme
yapısına
bağlı
olarak
meme
kanseri
açısından
yüksek
risk
taşımaktadır.
Genç
yaşta
Hodgkin
lenfoma
nedeniyle
radyoterapi,
Mamografide
yoğun
memeye
sahip
kadınlar,
meme
biyopsi
sonrası
atipik
duktal
veya
lobar
hiperplazi
olanlar
ile
in
situ
lobüler
karsinom
olanlar
(4
kat
fazla
risk), anne karnında DESe maruziyet (2 kat risk)
Genetik mutasyonu olan hastalarda tarama
BRCA
mutasyonu
olan
kadınlarda
daha
erken
ve
sık
tarama
yapılmalıdır.
Bu
hastalarda
70
yaşına
kadar
meme
kanseri
gelişme
riski
%40
ile
85
arasında
değişmektedir.
25-29
yaş
arasında
6
ay
ile
yıllık
klinik
meme
muayenesi
ve
yıllık
kontrastlı
MR
ile
görüntüleme
yapılmalıdır.
30
yaş
üzerinde
6
aylık
süreler
ile
yıllık
mamografi
ve
yıllık
MR
yapılmalı,
yıllık
meme
muayenesi
de
yapılmalıdır.
Hasta
ile
bilateral
mastektomi
tartışılmalı, bu sayede meme kanseri riski %85 ile 100 arasında azaltılabilir.
Risk faktörleri ve önleme
Yaş
ile
beraber
risk
artmaktadır.
Genel
olarak
meme
kanseri
teşhisi
alan
hastalarda
belirgin
bir
risk
faktörü
bulunmamaktadır.
Ailede
meme
over
veya
kalıtımsal
meme
over
kanseri
sendromu
ile
ilişkili
diğer
kanserlerin
bulunması
(prostat-
pankreas
gibi),
bilinen
gen
mutasyonu
atipik
hiperplazi
veya
in
situ
lobüler
karsinom,
erken
menarş,
geç
menopoz,
nulliparite,
menarş
ile
ilk
gebelik
arasındaki
sürenin
uzun
olması,
östrojen
ve
progesteron
içeren
hormon
replasman
tedavisi,
emzirme
yapılmaması,
ileri
yaş,
bazı
etnik
gruplar
(Askenazi),
yüksek
vücut
kitle
indeksi, alkol ve sigara kullanımı, mamografide yoğun meme, radyoterapi öyküsü.
Serviks kanseri
1975'ten
2011'e
servis
kanseri
insidansında
%50
azalma
izlenmiştir.
Yeni
vakaların
çoğunluğu
uygun
tarama
yapılmayan hastalarda rastlanmaktadır.
Serviks
kanseri
taraması
21
ile
65
yaşı
arasında
yapılması
önerilmektedir.
21
ile
29
yaşları
arasında
tarama
3
yılda
bir
sitoloji,
30
yaş
üzerinde
sitoloji
ve
HPV
nin
birlikte
yapılmasını
önerilmektedir.
30
yaşından
sonra
5
yılda bir kotest veya 3 yılda bir sitoloji ile tarama yapılabilir.
Tarama kılavuzları
Tarama seçenekleri sitoloji, yüksek riskli HPV ya da kotest şeklindedir
2018'de
yayınlanan
USPSTF
kılavuzuna
göre
30-65
yaş
arası
kadınlarda
yalnız
yüksek
riskli
HPV
taraması
önerilmektedir.
Tarama
21
yaşından
sonra
başlanmalı
ilk
ilişki
yaşı
ve
diğer
davranışsal
faktörler
tarama
başlama
yaşını
değiştirmemektedir.
21
ile
29
yaş
arasında
yalnız
sitoloji
ile
tarama
yapılmalıdır.
Refleks
HPV
testi
normal
sitoloji
sonuçlarında
kullanılabilir.
30
ile
65
yaş
arasında
5
yılda
bir
kotest,
3
yıl
arayla
sitoloji
veya
HPV testi uygulanabilir. ACOG’a göre kotest tercih edilmelidir.

TJOD
İstanbul Şubesi


TJODist
Bülteni
USPSTF
3
yönteminde
eşit
olduğunu
ve
HPV
ile
taramanın
5
yıl
aralıklarla
yapılması
gerektiğini
belirtmektedir.
FDA
onaylı
yalnız
bir
primer
HPV
tarama
testi
bulunmaktadır.
Tarama
65
yaşından
sonra
kesilebilir.
10
yıl
uygun
tarama
sonuçları
gereklidir.
Son
sitoloji
5
yıl
içerisinde
olmalıdır.
Yeni
cinsel
partner
bu
durumu
değiştirmez. HPV aşısı tarama kılavuzlarında değişiklikler yapmamaktadır.
Özel popülasyonlar
CİN 2-3, adenokarsinom in situ öyküsü olan hastalarda tedavi sonrası tarama 20 yıl devam etmelidir.
HİV
teşhisi
olan
hastalarda
tarama
sıklaştırmalıdır.
21
yaşından
önce
cinsel
ilişkiye
başlamışsa
veya
seksüel
aktif
hastada
HİV
teşhisi
bir
yıl
içerisinde
konulmuşsa
taramaya
başlanmalıdır.
ilk
3
yıl
yıllık
HPV
taraması
yapılmalı,
sonuçlar
negatif
ise
tarama
3
yıla
çıkarılabilir.
30
yaşından
önce
sadece
sitoloji
ile
tarama
önerilmektedir.
30
yaşından
sonra
kotest
veya
sitoloji
ile
tarama
yapılabilir.
Tarama
65
yaşından
sonra
da
devam etmelidir.
İmmünbaskılanmış
bireylerde
tarama
ACOG’a
göre
yıllık
sitoloji
ile
taramadır.
Anne
karnında
DES’e
maruziyeti
olan kadınlarda yıllık sitoloji yapılmalıdır. Sitoloji serviks ve üst 1/3 vajinadan alınmalıdır.
Histerektomi sonrası tarama:
Servikal
displazi
hikayesi
olmayan
total
histerektomi
kadınlarda
tarama
sonlandırılabilir.
CİN
2
ve
üzeri
displazi
hikayesi
olan
kadınlar
tedavi
sonrası
en
az
20
yıl
taramaya
devam
edilmelidir.
ACOG’a
göre
3
yıl
arayla
sitoloji
vajinal
güdükten
alınmalıdır.
Supraservikal
histerektomi
yapılan
kadınlar
standart
servikal
kanser
taramasına
tabidirler.
Risk faktörleri ve korunma
Güvenli
cinsel
pratik,
prezervatif
kullanımı,
partnerlerin
geçmiş
cinsel
hastalıklar
ile
ilgili
bilgi
vermesi,
seks
oyuncaklarının
uygun
temizliği
önemi
anlatılmalıdır.
Tarama
kılavuzlarını
uyum
HPV
aşısı
ve
yüksek
riskli
davranışlardan sakınma korunmada en önemli basamaklardır.
Sigaranın
servikal
hastalıklara
etkisi
anlatılmalıdır.
HPV
aşısı
11-12
yaşındaki
kız
ve
erkek
çocuklarına
yapılması önerilir. FDA aşıya 45 yaşına kadar kullanımına onay vermiştir.
Kolorektal kanser
Kolorektal
kanserler
50
yaş
altındaki
insidansı
artmaktadır.
Bunun
sebebi
bilinememektedir.
Kolorektal
kanser
önlenebilir ve tedavi edilebilir bir kanser türüdür.
Tarama kılavuzları
Taramada kullanılabilen seçenekler:
Gaitada
gizli
kan,
Gaitada
immünohistokimyasal
test
(FİT),
Sigmoidoskopi,
Kolonoskopi,
Dışkıda
DNA
testi,
BT
kolonografi, kapsül kolonoskopi.
USPSTF’nin
önerisi
kadınların
50
ile
75
yaş
arasında
gaitada
gizli
kan,
sigmoidoskopi
veya
kolonoskopi
ile
taranmasıdır.
10
yılda
bir
kolonoskopi
ya
da
bunu
kabul
etmeyen
hastalarda
yıllık
gaitada
immunokimyasal
test. 5 yılda bir kolonoskopi 3 yılda bir DNA testi 5 ile 10 yıl arasında sigmoidoskopi, kapsül kolonografi.
Ayrıca
1.
derece
akrabalarında
60
yaşından
sonra
kolorektal
karsinom
veya
adenom
tespit
edilen
kişilerde
tarama
10
yılda
bir
40
yaşında
başlanmalıdır.
Ailesel
kolorektal
kanseri
olanlar
1.
Derece
akraba
arasında
60
yaşından
önce
kanser
olanlar
40
yaşından
önce
veya
hasta
hastalığa
yakalanan
en
genç
akrabasından
10
yıl
önce başlanmalıdır.
Amerikan kanser derneğine göre uygun tarama;
Yıllık
gaitada
immunokimyasal
test,
yıllık
gaitada
gizli
kan,
3
yılda
bir
gaitada
DNA
testi,
10
yılda
bir
kolonoskopi, 5 yılda bir BT kolonografi, 5 yılda bir sigmoidoskopidir.
Tarama testinde pozitiflik saptanırsa hastaya kolonoskopi yapılmalıdır.

TJOD
İstanbul Şubesi


TJODist
Bülteni
Risk faktörleri ve korunma
Kişisel
veya
ailesel
polip
veya
kanser
öyküsü,
inflamatuar
barsak
hastalığı,
genetik
durumlar,
radyoterapi
ve
kistik
fibrozis
kolorektal
kanser
için
yüksek
risklidir.
Bu
grup
hastada
tarama
erken
başlanmalıdır.
Sigara
ve
alkol
tüketilmemesi,
sağlıklı
bir
diyet,
kırmızı
ve
işlenmiş
etlerin
azaltılması,
yüksek
fiber,
kalsiyum,
meyve
ve
sebze
tüketilmesi,
düzenli
egzersiz,
aspirin
ve
hormon
replasman
tedavisi
kolorektal
kansere
karşı
koruyucudur.
Akciğer kanseri
Akciğer
kanserinin
en
sık
nedeni
sigaraya
maruziyettir.
30
paket/yıl
sigara
kullanan
veya
15
yıl
içerisinde
sigarayı bırakan kadınlarda tarama yapılmalıdır.
Tarama kılavuzları
Taramada
ilk
yapılan
çalışmalarda
akciğer
filmi,
balgam
sitolojisi,
biyolojik
belirteçler
kullanılmıştır.
Fakat
bu
tarama
yöntemleri
ile
ölümlerde
azalma
görülmemiştir.
2011
yılında
ulusal
akciğer
tarama
çalışmasında
düşük
dozlu
Toraks
BT
ile
taramada
mortalitede
azalma
gözlemlenmiştir.
USPSTF
55
ile
80
yaş
arasında
sigara
kullanan veya 15 yıl içerisinde sigarayı bırakan kadınlara düşük doz toraks BT ile tarama önerilmektedir.
Risk faktörleri ve korunma
Sigaraya
maruziyet
ilerleyen
yaş
radon
aile
hikayesi
asbest
ve
arsenik
KOAH
ve
pulmoner
fibrozis
risk
faktörleridir
Over kanseri
En
ölümcül
jinekolojik
kanserdir.
Yaşam
boyu
over
kanserine
yakalanma
ihtimali
1/78’dir.
Tanıda
medyan
yaş
63’tür. WPSI ortalama riskli bir kadında over kanseri taramasını önermemektedir.
Tarama kılavuzları
Hiçbir
kılavuzda
tarama
önerilmemektedir.
Transvajinal
ultrason,
Ca125
ve
pelvik
muayene
ile
mortalitede
azalma
izlenmemiştir.
Yapılan
birçok
çalışmada
tarama
ile
gereksiz
ameliyat
ve
işleme
neden
olduğu
gösterilmiştir.
UKCTOC
çalışmasına
göre
1
kanseri
yakalayabilmek
için
10
gereksiz
cerrahi
yapılmaktadır.
Şişkinlik, erken doyma, pelvik veya abdominal ağrısı olan kadınlarda ultrason ve serum testi yapılabilir.
Yüksek riskli popülasyon
BRCA
mutasyonlu,
Lynch
sendromlu
veya
bazı
genetik
anomalileri
olanlarda
tarama
yararlı
olabilir.
30
yaşından
önce
bu
grup
hastaya
tarama
yapılmamaktadır.
ACOG’a
göre
30-35
yaşından
başlayarak
TV-USG
ve
Ca125
ile
tarama
yapılabilir.
Çocuk
isteği
olmayan
veya
40
yaşından
sonra
risk
azaltıcı
BSO
önerilmektedir.
Over kanser riskini %80 azaltabilmektedir.
Risk faktörleri ve korunma
Meme
kanseri
olan
kadınların
yaşamları
boyunca
%30’u
over
kanserine
yakalanmaktadır.
Bu
risk
40
yaş
altında
daha
yüksektir.
Sigara,
HRT,
obezite,
talk
pudrası
ve
artmış
boy
risk
faktörleridir.
Gebelik,
sterilizasyon
ve OKS kullanımı riski azaltmaktadır.

TJOD
İstanbul Şubesi
Stres
üriner
inkontinans
kadınların
yaklaşık
%25’i
etkilerken,
hayat
kalitelerini
de
olumsuz
yönde
etkilemektedir.
Kadınların
büyük
bir
kısmı
için
cerrahi
olmayan
tedaviler
arasında
yer
alan
pelvik
taban
egzersizleri
ve
pesser
gibi
inkontinans
cihazları
etkinliği
gösterilmiş,
yararlı
seçenekler
olarak
görülmekteyken,
bir çok kadın da daha etkin tedavi olarak gördükleri cerrahi tedaviyi talep etmektedirler.
Ürojinekoloji
alanında
kullanılan
cerrahi
meşler
ile
ilgili
FDA
2011
güncellemesi,
Kanada
Sağlık
Danışma
Kurulu
2014,
İskoç
Bağımsız
Değerlendirme
2017’de
de
altı
çizildiği
gibi
olası
geri
dönüşsüz
komplikasyonların
olabileceği
hakkında
aydınlatılmış
onam
gereği
ve
bu
komplikasyonların
mutlaka
bildirilmesi
gerekliliği
sonrasında
meşler
önemli
bir
medya
ilgisi
ile
karşı
karşıyadır.
Her
ne
kadar
ehil
ellerde
bu
tedavi
seçeneğini
seçmiş
kadınlarda
midüretral
slingler
mükemmel
sonuçlar
verse
de
bu
medya
ilgisi
sonrasında
bazı
hastalarda
meş
veya
sling
işlemlerinden
kaçınma
cevabı
ortaya
çıkmıştır.
Bu
yazıda
bahsedilen
midüretral
slingler
sadece
retropubik
ve
transobturator
yaklaşımları
içermekte
olup,
uzun
dönem
sonuçları
ve
güvenilirlik
bilgisi
kısıtlı
olan
tek
insizyonlu
slingleri
(mini-sling)
içermemektedir.
Amerikan
Ürojinekoloji
Derneği
(AUA),
Uluslararası
Ürojinekoloji
Birliği
(IUGA)
ve
Kanada
Ürojinekoloji
Derneği
gibi
çok
sayıda
organizasyon
stres
üriner
inkontinansta midüretral slinglerin kullanımını desteklemektedir.
Midüretral
slingler
1990’lı
yıllarda
kadın
stres
üriner
inkontinansını
tedavi
etmek
için
geliştirlen
minimal
invazif
bir
yöntemdir.
Bu
işlem
ile
birlikte
midüretra
seviyesine
kalıcı
bir
tip
1
polipropilen
meş
bandı
konularak
dinamik
üretral
destek
sağlanmaktadır.
Dünya
çapında
en
sık
uygulanan
inkontinans
işlemi
olan
midüretral
slingler
ayrıca
en
geniş
çalışılmış
stres
inkontinans
cerrahisidir.
Çok
sayıda
çalışmada
5
yıla
kadar
olan
etkinliğinin
%80’lerin
üzerinde
olduğu
ve
uzun
dönem
etkinliğinin
diğer
stres
inkontinans
cerrahisi
işlemlerine
göre
daha
üstün
olduğu
gösterilmiştir.
Ayrıca
her
ne
kadar
küçük
bir
gurup
olsa
da
17
yıllık
yüksek
etkinlik
kanıtı
ile
izlendiği
bilinmektedir.
Midüretral
sling
işlemleri
çoğunlukla
vaginal
yoldan
yapılan
prolapsus
tamirleri
ile
kombine edilebildiğinden her iki durumda minimal invazif olarak cerrahi yoldan tedavi edilebilmektedir.
Geleneksel
otolog
pubovaginal
sling
veya
Burch
kolposüspansiyonu
gibi
meşsiz
cerrahiler
ile
karşılaştırıldığında
midüretral
slingler
benzer
veya
daha
başarılı
işlemler
olarak
rapor
edilirken,
kısa
operasyon
zamanı
ve
normal
günlük
aktivitelere
dönüşün
daha
erken
gerçekleşmesi
en
önemli
avantajlarındandır.
Her
cerrahi
işlemde
olabileceği
gibi
komplikasyon
riskleri
vardır
ancak
tabloya
bakıldığında
bu
oranlar
oldukça
düşük
olup,
alternatif
meş
kullanılmayan
işlemlere
göre
de
daha
az
komplikasyon
oranına
sahiptir.
Meş
ile
ilgili
görülen
komplikasyonlar
hariç,
tüm
inkontinans
işlemlerinde
görülebileceği
gibi
işeme
disfonksiyonu,
meş
erozyonu,
akut
ağrı,
kronik
pelvik
ağrı,
infeksiyon,
disparoni,
kanama,
nöromüsküler
hasar,
organ
hasarı
ve
nüksler
komplikasyonlar
ortaya
çıkabilmektedir.
Retropubik
işlemlerde
daha
fazla
mesane
perforasyonu
ve
işeme
disfonksiyonu
gibi
komplikasyonlar
görülürken
transobturator
slinglerde
de
daha
fazla
kasık
ağrısı
meydana
gelmektedir.
Midüretral
slingler
sonrası
gelişen
komplikasyonlar
nedeniyle
yaklaşık
kadınların
%3’ünde
tekrar
operasyon
gerekliliği
ortaya
çıkmaktadır.
Ancak
bazen
komplikasyonlar
tamamen
geri
dönüşümlü
olmayabilmektedir.
Midüretral
sling
işlemlerinden
önce
alternatif
tedavi
seçenekleri
ve
olası
cerrahi
riskler
ile
ilgili
danışmanlık
hizmeti
onamın
rutin
bir
parçası
olmalıdır.
Cerrahın
işlem
hacmine
göre
sonular
ve
komplikasyon
oranları
etkilendiğinden
bu
işlemleri
yapan
kişilerin
cerrahi
komplikasyonların
ve
başarı
oranlarının düzenli aralıklarla gözden geçirildiği kalite ve hasta güvenliği mekanizmaları olmalıdır.
Kanada
Jinekoloji
ve
Obstetri
Derneği,
aydınlatılmış
onamı
alınmış
hastalarda
eğitilmiş
cerrahlar
tarafından
yapılan
stres
üriner
inkontinans
cerrahi
yönetiminde
hem
retropubik
hem
de
transobturator
yoldan
monofilaman polipropilen midüretral slingin kullanılmasını önermektedir.


TJODist
Bülteni
STRES ÜRİNER İNKONTİNANS İÇİN MİDÜRETRAL SLİNGLER KOMİTE GÖRÜŞÜ
NO.387
Özetleyen: Dr. Cenk Yaşa

COMMITTEE OPINION NO 387- MID-URETHRAL SLINGS FOR STRESS URINARY INCONTINENCE
J Obstet Gynaecol Can 2019;41(9):1389−1391

TJOD
İstanbul Şubesi
Antifosfolipid
sendromu
(APS),
antifosfolipid
antikorların
(aPL)
varlığıyla
karakterize
otoimmün
bir
hastalıktır.
Güncel
olarak
sınıflama
kriterlerine
dahil
olan
antikorlar,
lupus
antikoagülanı
(LA),
antikardiyolipin
antikorlar
(aCL)
ve
anti-β2-glikoprotein
1
(β2GP1)
antikorlarıdır.
APS,
venlerde,
arterlerde
ve
mikrovasküler
tromboz
ve
obstetrik
komplikasyonlar
gibi
pek
çok
klinik
fenotip
ile
kendini
gösterebilir.
Obstetrik
APS’daki
(OAPS)
gebelik
komplikasyonları,
açıklanamayan
tekrarlayan
erken
gebelik
kayıpları,
fetal
ölüm
veya
ağır
preeklampsi,
eklampsi,
intrauterin
gelişme
kısıtlılığı
ya
da
plasental
yetmezliğin
diğer
sonuçlarına
bağlı
erken
doğum
olarak
sıralanabilir.
Aspirin
ve
heparin
kullanımı
ile
birlikte
gebelik
takibinin
dikkatlice
ve
iyi
gözlemlenerek
yapılması,
obstetrik
APS’de
gebelik
sonuçlarını
iyileştirir
ve
günümüzde
APS’u
olan
kadınların
yaklaşık
%70-80’inin
başarılı
gebelik
sonuçları
olduğu
görülmektedir.
Ancak,
mevcut
bakım
standartları
tüm
gebelik
komplikasyonlarını
önlemez,
çünkü
APS
gebeliklerin
%20-30’unda
tedavi
başarısızlığı
görülür.
Günümüzde
diğer
tedavi
seçenekleri
araştırılmaktadır
ve
retrospektif
çalışmalar,
hidroksiklorokin
ve
olasılıkla
pravastatin
tedavilerinin,
aPL
taşıyan
gebe
kadınlarda
verilmesi
gerektiğini
göstermiştir.
Bu
derlemede,
OAPS’un
güncel
tedavi seçeneklerine odaklanılmıştır.
1.
Giriş
Antifosfolipid
sendromu
(APS),
lupus
antikoagülan
(LA),
antikardiyolipin
antikorlar
(aCL)
ve
anti-β2-glikoprotein
1
antikorların
(β2GP1)
gibi
antifosfolipid
antikorların
(aPL)
varlığıyla
karakterize
otoimmün
bir
hastalıktır.
Hastalarda,
bu
üç
antikor
alt
grubunun
biri,
ikisi
veya
hepsi
pozitif
olabilir.
Her
hastada,
tüm
antikorların
değerlendirilmesi
önemlidir.
Sonuçta,
pozitif
antikor
testlerinin
sayısı
“tek”,
“çift”
veya
“üçlü”
pozitif
olarak
adlandırılır.
APS
sınıflama
kriterleri
sıklıkla
tanıya
da
rehberlik
eder.
Orijinal
olarak
Sapporo
kriterlerinde
vurgulanmış, 2006’da güncellenmiştir ve şimdi Sydney kriterleri olarak bilinmektedir.
Dolaşımdaki
LA
ve
aCL,
tromboz,
gebelik
kaybı
ve
trombositopeni
ilişkisi,
ilk
olarak
sistemik
lupus
eritematozus
(SLE)
hastası
kadınlarda
tanımlanmıştır.
SLE
hastaları
“sekonder”
olarak
adlandırılmıştır,
ancak
günümüzde
APS’nun
kendi
başına
otoimmün
bir
hastalık
olduğu
yaygın
olarak
kabul
görmüştür
ve
sekonder
teriminde vazgeçilmiştir.
APL
varlığı
,
majör
edinilmiş
bir
trombofilidir
ve
venöz
tromboz,
arteryel
tromboz
ve
mikrovasküler
tromboza
yatkınlık oluşturur.
APS’nin
ayırt
edici
özelliği,
açıklanamayan
tekrarlayan
erken
gebelik
kayıpları,
fetal
ölüm
veya
intrauterin
gelişme
kısıtlılığı
(IUGR),
preeklampsi
toksemisi
(PET),
eklampsi,
ya
da
plasental
yetmezliğin
diğer
sonuçlarına
bağlı
erken
doğum
olarak
sıralanabilir.
aPL,
tekrarlayan
birinci
trimester
kayıplarının
yaygın
bir
nedenidir;
tekrarlayan
birinci
trimester
gebelik
kayıpları
öyküsü
olan
500
kadını
içeren
retrospektif
tek
merkezli
bir
kohort
çalışmasının
verileri,
olguların
%26,4’ünün
aPL
varlığıyla
ilişkili
olduğunu
göstermiştir.
aPL,
ağır
PET
ve
ölü
doğumla
da
sıkça
ilişkillidir,
ağır
PET
olan
kadınların
%12’sinde
ve
ölü
doğum
olgularının
%11’inde
saptanır.
Günümüzde,
önleyici
APS
tedavisi
standart
olarak,
antikoagülasyon
ve
antitrombosit
tedavisi
verilmesine
dayanır.
Heparin
(anfraksiyone
heparin
(AF)
veya
düşük
moleküler
ağırlıklı
heparin
(DMAH))
ve
düşük
doz
aspirin
(DDA)
verilmesi,
%70-80
canlı
doğum
oranı
ile
sonuçlanmıştır,
ancak
bazı
çalışmalarda
DMAH
ile
canlı
doğum oranlarında herhangi bir gelişme olmadığı gösterilmiştir.


TJODist
Bülteni
GEBELİKTE ANTİFOSFOLİPİD SENDROMUNUN YÖNETİMİ
Managing antiphospholipid syndrome in pregnancy Volume 181, Supplement 1, September 2019, 41-46
Özetleyen: Dr. Hakan Erenel

Link https://www.ncbi.nlm.nih.gov/pubmed/31477227

TJOD
İstanbul Şubesi
Daha
yeni
veriler,
antimalaryal
hidroksiklorokin
ve
pravastatin
gibi
yeni
ilaçların
rolüne
işaret
etmektedir
ve
bu
nedenle,
bu
gözlemi
doğrulamak
için
prospektif
randomize
kontrollü
çalışmalara
ihtiyaç
vardır.
Lefkou
ve
ark.,
retrospektif
tek
merkezli
bir
olgu
kontrol
çalışmasında,
aPL
ile
ilişkili
PET
ve/veya
IUGR
tablosu
olan,
DDA
ve
DMAH
ile
standart
tedavi
alan
kadınlarda
pravastatinin
olası
faydalı
etkilerine
vurgu
yapmışlardır.
Ayrıca,
antimalaryal
hidroksiklorokin
(HCQ)
de,
obstetrik
ve
trombotik
APS’de
ilgi
odağı
haline
gelmiştir
ve
European
Medicines
Agency
(Avrupa
Tıp
Birliği)
(EMA)
APS
tedavisinde
HCQ’e
lisans
vermiştir.
Retrospektif
veriler,
HCQ’in
APS’de
tromboz
riskini
azalttığını
göstermektedir.
İki
retrospektif
çalışmada
aPL
ile
ilişkili
gebelik
komplikasyonları
olan
kadınlarda
HCQ
kullanımının
gebelik
sonuçlarının
iyileşmesi
ile
ilişkili
olduğu
görülmüştür.
Tercih
edilen
bir
güvenlik
profiline
sahip
olan
HCQ,
günümüzde
uluslararası
olarak,
gebelik
boyunca
sistemik
lupus
eritematozus
için
immün
modülasyon
gereksinimi
olan
hastalara
önerilmektedir.
Ancak,
acil
olarak,aPL
olan
kadınlarda
HCQ’nin
rolünü
değerlendiren
randomize
kontrollü
çalışmalara
ihtiyaç
vardır
ve
devam
eden
HYPATIA
çalışmasının
(gebelikteki
randomize
kontrollü
çalışma)
sonuçları
hevesle
beklenmektedir.
2.
Patogenez
2.1
Tromboz
aPL’ların,
arteryel
ve/veya
venöz
dolaşımda
ve/veya
mikrodolaşımda
trombüs
oluşumunu
indükleme
becerisi
vardır.
Ancak,
aPL’ların
tam
olarak
hangi
mekanizma
ile
tromboza
yol
açtığı
tam
olarak
açıklanabilmiş
değildir.
aPL’ların,
endotelyal
hücreler,
trombositler
ve
monositler
gibi
immün
hücreler
de
dahil
olmak
üzere,
hemostaz
sürecine
dahil
olan
bazı
hücreleri
aktive
etme
potansiyeli
vardır.
Diğer
çalışmalar,
bazı
aPL’ların
fibrinolizisi
ve
protein C yolağını inhibe ettiğini göstermiştir.
2.2
Gebelik komplikasyonları
aPL
ile
ilişkili
tekrarlayan
ilk
trimester
gebelik
kayıplarının
patogenezi,
geç
gebelikte
oluşan
morbiditenin
patogenezinden
farklıdır.
İlk
trimester
gebelik
kayıpları,
aPL’ların
doğrudan
büyüme
ve
plasentasyon
üzerine
olan
inhibitör
etkisi
ile
trofoblast
hücrelerinin
apoptozisinden
kaynaklanırken;
PET,
IUGR
ve
ölü
doğum
gibi
geç
obstetrik
tablolar,
trombotik
ve
inflamatuar
değişikliklere
bağlı
plasental
disfonksiyondan
kaynaklanır.
Bu
sonuçların
altında
yatan
olası
nedenler,
preeklampside
olduğu
gibi,
plasentaya
maternal
kan
akımını
azaltıp
hipoksik
hasar
gelişmesine
yol
açan
ekstravillöz
spiral
arterlerin
gelişiminde
yetersizlik,
fetusa
yeterli
besin
iletilememesi ve plasentaya zarar veren yüksek velositeli ve yüksek basınçlı kan akımıdır.
3.
Klinik tablolar
3.1
Trombotik APS
APS,
herhangi
bir
vasküler
yatakta
tromboz
gelişimine
neden
olan
eşsiz
bir
trombofilidir.
En
sık
görülen
arteryel
tablolar,
inme
veya
geçici
iskemik
ataklar
gibi
nörolojik
tablolardır,
diğer
yandan
en
sık
venöz
tromboembolik tablolar derin ven trombozu (DVT) ve pulmoner emboli (PE) gibi durumları kapsar.
Retinal
arter
veya
ven
trombozu,
amaurosis
fugax,
renal
trombotik
mikroanjiyopati,
pulmoner
hipertansiyon
ve
vasküler
demans
gibi
diğer
tablolar
daha
nadirdir
(hastaların
<%10’nda).
Adrenal
tromboz,
avasküler
nekroz,
kemik
infarktları
veya
Budd-Chiari
Sendromu’na
bağlı
patolojik
kemik
kırıkları
gibi
tablolar
daha
da
nadirdir
(%1’inde
görülür).
Livedo
retikülaris,
en
sık
görülen
cilt
tablosudur
ve
bazen
beyindeki
oklüzif
arteryel
olaylarla
(Sneddon sendromu olarak da bilinen) ilişkilidir.
En
ciddi
klinik
tablo
çok
nadir
görülür
ve
katastrofik
APS
(CAPS)
olarak
bilinir.
CAPS,
sıklıkla
kısa
sürede
gelişen
küçük
damar
trombozunun
eşlik
ettiği
en
az
üç
organda
görülen
tromboz
olarak
sınıflandırılır
ve
%50’nin üzerinde mortalitesi vardır.
3.2
APS’nin diğer tabloları
Trombotik
olmayan
APS
tabloları,
sıklıkla
kanama
komplikasyonlarıyla
değil
tromboz
riskiyle
ilişkili
olan
trombositopeni
ve
kardiyak
kapak
anormalliklerini
(hafif
kalınlaşma
ve/veya
kapak
trombozuna
bağlı
yetmezlik)
içerir.
Gebelik
protrombotik
bir
durumdur
ve
bu
nedenle,
geçirilmiş
tromboz
öyküsü
olanlarda,
tekrarlayan


TJODist
Bülteni

TJOD
İstanbul Şubesi
trombozu
önlemek
için
tromboprofilaksi
verilir.
APS’ye
bağlı
en
şaşırtıcı
durumlardan
biri,
trombozun,
orijinal
tromboz
ile
aynı
vasküler
yatakta
gelişme
eğiliminde
olmasıdır;
başka
bir
deyişle,
geçirilmiş
inme
öyküsü
olanlarda
yeniden
inme
gelişme
ve
geçirilmiş
derin
ven
trombozu
(DVT)
öyküsü
olanlarda
yeniden
DVT
gelişme riski yüksektir.
3.3
Obstetrik APS
3.3.1
Tekrarlayan erken gebelik kayıpları
Avrupa’da
erken
düşük
için
en
sık
kullanılan
tanım,
konsepsiyondan
sonraki
ilk
12
haftada
gerçekleşen
gebelik
kaybıdır.
Klinik
olarak
tanı
konan
gebeliklerin
yaklaşık
%15’i
bu
şekilde
tamamlanır.
Erken
düşüğün
ve
tekrarlayan
düşüğün
pek
çok
nedeni
vardır;
bunlar,
genetik
anormallikler,
anatomik
varyasyonlar,
endokrin
veya
immün
faktörler
(tiroid
hastalığı
da
dahil
olmak
üzere),
enfeksiyonlar
(en
sık
“TORCH”
tarafından
kaynaklananlar; örn, toksoplazmozis, diğer, rubella, sitomegalovirus, herpes simpleks virüs) ve aPL’lardır.
Gerçekte,
aPL’lar,
tekrarlayan
erken
düşüklerin
en
sık
tedavi
edilebilir
nedeni
olarak
bilinir.
Tekrarlayan
düşük
öyküsü
olan
500
kadından
oluşan
bir
kohortta,
Rai
ve
arkadaşları,
kadınların
%9,6’sında
LA’nın
kalıcı
olarak
pozitif
olduğu,
buna
karşılık
aCL
IgG
ve
IgM’in
sırasıyla
%3,3
ve
%2,2’sinde
pozitif
olduğu
bulunmuştur.
Tekrarlayan
erken
gebelik
kayıplarının
önlenmesi,
obstetrik
APS’de
tedavinin
randomize
kontrollü
çalışmalar
dahil bazı klinik çalışmalara dayandığı tek alandır.
3.3.2
Geç gebelik kayıpları
Geç
gebelik
kaybı
veya
fetal
ölüm,
10.
gebelik
haftasından
sonra
yaşanan
gebelik
kaybıdır.
Ölü
doğum
kimilerine
göre
20
haftadan
sonra
yaşanan
kayba
işaret
eder;
WHO
tarafından
uluslararası
ölçekte
önerilen
ve
bizim
kliniğimizde
de
kullanılan
tanıma
göre
ise,
28.
gebelik
haftasından
sonra
bebeğin
herhangi
bir
hayati
bulgu
olmaksızın
dünyaya
gelmesidir.
Yapılan
tek
popülasyon
temelli
çalışmada
(ölü
doğum
iş
birliği
araştırma
ağı),
20.
Gebelik
haftasından
sonra
gerçekleşen
582
fetal
ölüm
olgusunda,
aPL’lar
(aCL
ve
anti-β2GP1)
ile
artmış
ölü
doğum
oranı
(3-5
kat)
arasında
ilişki
olduğu
bildirilmiştir.
Ancak,
grupta
lupus
antikoagülanı
ölçülmemiştir ve aPL’ların kalıcılığını doğrulamak için 12 hafta sonra aCL’lar yeniden değerlendirilmemiştir.
3.3.3
Plasental yetmezlik ve preeklampsi toksemisi (PET)
Plasental
yetmezlik,
plasentanın
gelişmekte
olan
fetusa
yeterli
besini
aktarmadaki
başarısızlığıdır.
Plasental
yetmezlik,
fetal
gelişme
kısıtlılığı
(FGK)
ve/veya
PET
ve/veya
plasenta
dekolmanı
olarak
kendini
gösterebilir.
FGK,
asıl
olarak
ilk
gebeliklerin
%2-8’inde
meydana
gelirken,
ağır
PET
gelişmiş
ülkelerdeki
gebeliklerin
%0,5’inde bulunur.
Prospektif
gözlemsel
çalışmaların
çoğu,
aPL
ile
PET
ve
plasental
yetmezlik
arasındaki
ilişkiyi
destekler.
Yakın
tarihli
bir
sistematik
derlemede,
orta-yüksek
düzeydeki
aCL’lerin
PET
ile
ilişkili
olduğu
gösterilmiştir.
Ayrıca,
bazı
prospektif
ve
retrospektif
çalışmalarda,
kalıcı
olarak
yüksek
titrede
aPL
varlığının,
FGK
ve
erken
doğumlarla
ilişkili
olduğu
gösterilmiştir.
Olgu
kontrol
çalışmalarından
elde
edilen
veriler,
PET
veya
FGK
öyküsü
olan
hastaların
%50’sinde
aPL
bulunduğu
saptanmıştır,
buna
karşılık
sağlıklı
gebe
kadınlarda
bu
oran
%7
veya
altındadır.
Bugüne
kadar,
aPL’ları
olan
kadınlarda
PET
ve
FGK’nın
yönetimi
ve
önlenmesini
değerlendiren
yalnızca
bir
randomize
kontrollü
çalışma
yapılmıştır.
Bu
çok
merkezli
çalışmanın
(FRUIT-RCT)
amacı,
kombine
DMAH
ve
aspirin
tedavisinin,
34.
gebelik
haftasından
önce
hipertansif
bozukluk
ve/veya
gebelik
haftasına
göre
küçük
(SGA)
bebek
nedeniyle
erken
doğum
öyküsü
olan
ve
APL’ları
olan
kadınlarda,
gebeliğin
hipertansif
bozukluklarının
(preeklampsi,
eklampsi
veya
HELLP
sendromu)
tekrarlama
olasılığını
azaltıp
azaltmadığını
değerlendirmektir.
Ne
yazık
ki,
çalışma
vaka
oranlarının
çok
düşük
olması
nedeniyle
sonlandırılmıştır
ve
33
kadının
(%50
risk
azalması
tespit
etmek
için
kurtarma
hedefi
85
olguydu)
son
değerlendirmesinde,
tek
başına
aspirin
veya
aspirin
DMAH
kombinasyonu
verilmesi
arasında
anlamlı
fark
olmadığı görülmüştür.
Tekrarlayan
plasenta
aracılı
gebelik
komplikasyonlarının
önlenmesinde
DMAH
verilmesi
ile
verilmemesinin
karşılaştırıldığı
yakın
tarihli
bir
metaanalizde,
plasenta
aracılı
gebelik
komplikasyonu
öyküsü
ola
848
gebe
kadında (aPL olan ve olmayan) DMAH lehine bulgu saptanmamıştır.


TJODist
Bülteni

TJOD
İstanbul Şubesi
4.
Gebelikte yönetim
4.1
Gebelik öncesi danışmanlık
Bilinen
aPL
ve
APS’u
olan
tüm
hastalara,
partnerleriyle
birlikte
gelecekteki
gebeliğin
yönetimini
tartışmak
ve
spesifik
riskleri
tanımlamak
için
gebelik
öncesi
danışmanlık
verilmelidir.
Bu,
Romatizmaya
Karşı
Avrupa
Birliği
(EULAR)’nin,
sistemik
lupus
eritematozus
ve/veya
antifosfolipid
sendromlu
hastalarda
aile
planlaması,
yardımcı
üreme,
gebelik
ve
menopoz
ile
ilgili
önerileriyle
de
uyumludur.
Bir
kadındaki
gebelik
riskleri,
geçmişteki
obstetrik
ve
trombotik
öyküsüne
bağlı
olduğu
için,
oldukça
çeşitli
öneriler
ortaya
çıkacaktır.
Örneğin,
bir
kadının,
kalıcı
aPL
varlığında,
geçmişte
sağlıklı
canlı
doğumları
olduysa,
gelecekteki
herhangi
bir
gebeliğinin
sonuçlarının
da
mükemmel
olacağı
ve
ilave
fetal
monitörizasyon
gerekmeyeceği
konusunda
hasta
rahatlatılabilir.
Tersine,
tekrarlayan
inme
öyküsü
olan,
INR
değeri
3-4
arasında
devam
eden,
24.
haftada
HELLP
sendromu
ve
prematüriteye
bağlı
uzun
dönem
sorunları
olan
bir
bebeğin
doğumuyla
sonuçlanan
bir
gebelik
öyküsü
olan
bir
hastaya,
aspirin
ve
DMAH
kullanımına
rağmen
gelecek
gebeliklerde
riskin
çok
yüksek
olduğu,
%5
tekrarlayan
inme
olasılığı
olduğu
ve
daha
ileri
düzeyde
tedavi
verilmeden
(ki
bu
da
deneysel
olarak) gelecek gebelikte HELLP sendromu gelişme olasılığının yüksek olduğu bilgisi verilmelidir.
Tüm
kadınlar
sigarayı
bırakmaları
ve
ulusal
gebelik
kılavuzlarına
göre
alkol
alımını
azaltmaları/kesmeleri
konusunda
cesaretlendirilmelidir.
Geçen
3
ayda,
özellikle
arteryel
trombotik
öyküsü
olan
ve/veya
kontrolsüz
hipertansiyonu
olan
hastalara
gebelik
planını
ertelemeleri
söylenmelidir.
Ağır
pulmoner
hipertansiyonu
olan
hastalara,
tablonun
ağırlaşma
ihtimalinin
çok
yüksek
olduğu
ve
anne
ölümü
oranının
%43
kadar
yüksek
olduğu
bilgisi verilerek hiç gebe kalmamaları gerektiği anlatılmalıdır.
Risk
düzeyinin
belirlenmesi
için
tam
bir
öykü
alınmalı
ve
aPL
profili
görülmelidir.
Ayrıca,
APS
hastalarının
üç
farklı
klinik
fenotipi
(tekrarlayan
erken
gebelik
kaybı
olanlar,
geçirilmiş
iskemik
plasental
komplikasyonları
olanlar
ve
geçirilmiş
maternal
trombozu
olanlar)
farklı
gebelik
sonuçlarıyla
ilişkilidir.
67
kadının
83
gebeliğinden
oluşan
bir
seride,
Bramham
ve
arkadaşları,
geçirilmiş
tromboz
öyküsü
olanların
neonatal
sonuçlarının,
10.
gebelik
haftasından
önce
tekrarlayan
gebelik
kaybı
öyküsü
olanlarla
kıyaslandığında
daha
kötü
seyrettiğini,
erken
doğum
oranlarının
(%26,8’e
karşı
%4,7,
p
=
0,05)
ve
gebelik
haftasına
göre
küçük
bebek
oranlarının
(%9,5’e
karşı
%4,8,
p
=
0.003)
daha
yüksek
olduğunu
belirtmişlerdir.
İnme
öyküsü
olan
hastalarda
gebelik
sonuçlarını
değerlendirmek
için
kısıtlı
veri
vardır.
Bir
prospektif
kohort
çalışmasında,
APS
ve
geçirilmiş
inme
ve/veya
geçici
iskemik
atak
öyküsü
olan
20
kadının
23
gebeliğinde,
düşük
doz
aspirin
ve
DMAH
tedavisine
rağmen 8 hastada preeklampsi, 3 hastada ise tekrarlayan inme geliştiği görülmüştür.
Gebelik
öncesi
vizitin
diğer
bir
amacı
da
tüm
ilaçlarının
gebelikte
kullanımının
güvenli
olduğuna
ikna
ederek
ilaç
kullanımını
mantıklı
hale
getirmektir.
Hastalar
400
µg
folik
asit
kullanmalı,
gebelikte
ihtiyacı
olan
hastalar
DMAH
ve
aspirin
desteği
almalı,
kendi
kendilerine
subkutan
enjeksiyon
yapmayı
öğrenmeleri
için
eğitim
verilmeli
ve
gebelik
testi
pozitif
olur
olmaz
warfarini
kesmeleri
tavsiye
edilmelidir.
Anti
Ro
antikorları
olanlara,
komplet kalp bloğu riskini azaltmak için gebelikten önce hidroksiklorokin başlanabilir.
4.2
Antenatal bakım
Antenatal
bakımın
özel
amacı,
özellikle
renal
trombotik
mikroanjiyopati
tabloları
olanlar
için
yakın
gözlem,
geçmişte
öyküsü
olanlar
için
gebelik
kaybının
önlenmesi
ve
preeklampsi
ile
fetal
gelişim
işaretlerinin
takip
edilmesidir.
Toplamda,
obstetrik
APS
olan
gebe
kadınlara
sıkı
bir
eğitim
verilmesi
ve
APS’ye
özel
ilgisi
olan
obstetrisyen,
romatolog
ve
hematologlardan
oluşan
multidisipliner
bir
ekip
tarafından
maternal
ve
fetal
sağlığın
takip edilmesi gerektiği konusunda uzlaşma sağlanmıştır.
Gebeliği
iyi
giden
tüm
APS
hastalarının
vajinal
doğum
yapabileceği
konusunda
obstetrisyenler
ve
anneler
rahatlatılmalıdır.
Vajinal
doğumda
postpartum
tromboz
riski
daha
düşüktür
ve
bebek
için
daha
sağlıklıdır.
Sezaryen doğum obstetrik nedenlerin varlığında düşünülmelidir.
Uterin
arterlerin
Doppler
değerlendirmesinde
zayıf
akım
görülmesi,
plasental
yetmezlik
ve/veya
preeklampsi
gelişmesi
açısından
indirekt
bir
belirteçtir.
APS’da,
20-24
haftada
normal
uterin
arter
değerleri,
kötü
fetal


TJODist
Bülteni

TJOD
İstanbul Şubesi
sonuçlar
açısından
yüksek
negatif
prediktif
değere
sahiptir.
20-24
haftada
bilateral
anormal
uterin
arter
değerleri
olan
APS’lu
gebe
kadınlarda,
fetal
gelişimi
ve
amniyotik
sıvıyı
değerlendirmek
ve
gerekliyse
end-
diyastolik
umblikal
arter
kan
akımını
değerlendirmek
için
obstetrik
ultrasonografi
yapılmalıdır.
APS’lu
33
kadında,
anormal
uterin
arter
Doppler
değerlerinin,
ilerideki
intrauterin
gelişme
kısıtlılığı
veya
preeklampsi
için
pozitif
prediktif
değeri
%67;
negatif
prediktif
değeri
ise
%93’tür.
100
gebeliği
kapsayan
diğer
bir
prospektif
çalışma
da
ikinci
trimester
Doppler
ultrasonografinin
sistemik
lupus
eritematozus
ve/veya
APS’da
geç
gebelik
sonuçlarını
en
iyi
öngören
araç
olduğunu
doğrulamıştır.
EULAR,
günümüzde
kılavuzlarına
uterin
arter
Dopplerinin kullanımını katmıştır.
4.3
Tekrarlayan trombozun önlenmesi
Gebelik
dışında
APS’un
trombotik
tablolarının
tedavisinde
ana
nokta,
K
vitamini
antagonisti
(VKA)
veya
heparin
ve
düşük
doz
aspirin
gibi
antitrombosit
tedaviyi
de
kapsayan
antikoagülasyona
dayanır.
Geçirilmiş
venöz
tromboembolizm
öyküsü
olan
APS
hastalarında
direkt
oral
antikoagülan
kullanımını
destekleyen
ön
veriler
mevuttur,
ancak
günümüzde
APS’de
direkt
oral
antikoagülan
kullanımı
ile
tekrarlayan
tromboz
oranlarının
yüksek
olduğunu
belirten
çok
sayıda
rapor
bulunmaktadır,
bu
nedenle
kullanımı
sınırlandırılmıştır.
Çok
nadiren
immün
modülatör
ajanlar,
immünsüpresyon
ve
antikompleman
tedaviler,
antitrombotik
ilaçlara
yanıt
vermeyen
hastalarda
veya
özellikle
CAPS
gibi
ciddi
durumlarda
kullanılabilir,
ancak
etkinliği
olduğuna
dair az kanıt bulunmaktadır.
Gebelikte,
aspirin
ve
DMAH’e
güvenilir.
DMAH,
K
vitamini
antagonistleri
ve
direkt
oral
antikoagülanlardan
farklı
olarak
plasentadan
geçmez.
Geçirilmiş
tromboz
öyküsü
olan
annelere,
olası
trombotik
olayları
önlemek
için
gebelik
boyunca
DMAH
ile
orta
veya
tam
doz
antikoagülasyon
uygulanır.
Bizim
antitrombotik
rejimimiz,
annenin
önceki
trombotik
öyküsüne
göre
belirgin
şekilde
değişkenlik
gösterme
eğilimindedir.
Genel
bir
kural
olarak,
geçmişte
arteryel
olay
öyküsü
olan
hastalarda
daha
yüksek
doz
DMAH
kullanıyoruz,
öte
yandan
annenin
bacağında
geçirilmiş
yalnızca
bir
DVT
öyküsü
varsa,
aspirinle
birlikte
sadece
tromboprofilaktik
dozda
DMAH
kullanıyoruz.
Eğer
trombotik
risk
yüksekse
DMAH,
doğumdan
hemen
sonra
warfarin
ile
değiştirilir
veya
annenin
meşguliyet
durumuna
göre
daha
uygun
olacaksa
DMAH
ile
devam
edilebilir.
K
vitamini
antagonistleri
ve heparinler emzirme ile uyumludur.
aPL
ve
APS
gebelikleri
ile
ilgili
süregiden
bir
endişe
de,
trombotik
renal
mikroanjiyopati
gelişme
olasılığıdır.
Bu
çok
korkulan
durum
nadir
görülür
ve
sıklıkla
hafif
proteinüri
ve/veya
hematürisi,
belki
artmış
kan
basıncı
ve
hafifçe
yüksek
kreatinini
olanlarda
insidental
olarak
gelişir.
DMAH
kullanımına
rağmen
gelişebilir
ve
yükselen
kreatinin değeri bir işaret olsa da klinik olarak PET’den ayrımı zor olabilir.
4.4
Obstetrik APS’un önlenmesi
Tekrarlayan
ilk
trimester
kayıplarına
bağlı
olarak,
obstetrik
APS
olan
kadınlarda
güncel
standart
bakım,
düşük
doz
aspirin
(75-100
mg/gün)
ve
düşük
doz
DMAH
veya
anfraksiyone
heparin
tedavilerini
içerir.
Bu
öneriler,
APS
olan
kadınlarda
sadece
düşük
doz
aspirin
ile
heparin
ile
birlikte
kombinasyon
tedavisini
karşılaştıran
üç
randomize
kontrollü
çalışmanın
sonuçlarına
dayanır.
Rai
ve
arkadaşları,
düşük
doz
aspirin
(DDA)
ve
anfraksiyone
heparin
(5000
ünite)
tedavisiyle,
tek
başına
düşük
doz
aspirin
tedavisine
kıyasla
canlı
doğum
oranlarının
daha
yüksek
olduğunu
(%42’ye
karşı
%71;
OR
3,37;
%95
CI
1,40-8,10)
göstermişlerdir.
Benzer
şekilde,
Kutteh,
tek
başına
DDA’e
karşı
DDA
ve
heparin
tedavisiyle
canlı
doğum
oranlarında
iyileşme
olduğunu
bildirmiştir
(%44’e
karşı
%80;
p<0.05).
Ancak,
DMAH
kullanan
diğer
iki
randomize
çalışmada
DDA’e
karşı
kombinasyon
tedavisiyle
sonuçlarda
farklılık
görülmemiştir
ve
her
iki
tarafta
da
canlı
doğum
oranları
%80’e
yakın
bulunmuştur.
Sonuçlardaki
bu
heterojenlik,
daha
önceki
iki
çalışmada,
yalnızca
DDA
alan
kadınlardaki
görece
kötü
sonuçlara
bağlanabilir.
Ayrıca,
gözlemsel
çalışmalardan
elde
edilen
veriler,
bu
alt
grupta
tek
başına
DDA
kullanımı
ile
gebelikte
%79-100
başarı
şansı
olduğunu
göstermiştir.
Obstetrik
APS’nin
tedavisi
için
güncel
öneriler,
tek
başına
DDA
başlanması
ve
eğer
tek
başına
DDA
gebelik
kaybı
ile
ilişkili
ise
DMAH
eklenmesidir.
Bu
yönetimi
destekleyen
veriler
yakın
zamanda
yayınlanmıştır.
Bramham
ve
arkadaşlarının
retrospektif
verileri,
ikinci
ve
üçüncü
trimester
gebelik
kaybı
olanlarda
aspirin
ve
DMAH
kullanımının
gebelik
sonuçlarını
olumlu
etkilediğini
göstermiştir.
Tablo
1,
farklı
klinik
durumlarda
APS
olan
kadınlar
için
tedavi
önerilerini göstermektedir.


TJODist
Bülteni

TJOD
İstanbul Şubesi
4.5
Postpartum
Geçirilmiş
tromboz
öyküsü
olan
tüm
kadınların,
postpartum
dönemde
DMAH
veya
K
vitamini
antagonisti
ile
antikoagülasyona
devam
etmesini
öneriyoruz.
Geçirilmiş
trombotik
APS
öyküsü
olmayan
kadınlar,
tromboemboli
risklerine
göre
değerlendirilmeli
ve
yerel
kılavuzlara
göre
endikasyon
varsa
tromboprofilaksi
almalıdır.
Lefevre
ve
arkadaşları,
DDA
ile
tedavi
edilseler
bile,
obstetrik
APS
olan
hastaların,
sağlıklı
kadınlara
kıyasla
daha
yüksek
trombotik
risk
taşıdığını
belirtmişlerdir
(3,3’e
karşı
0-0,5/100
hasta-yıl).
Benzer
şekilde,
temiz
obstetrik
öyküsü
olan
ve
tromboz
öyküsü
olmayan
1592
kadını
içeren,
10
yıllık
gözlemsel
bir
çalışmada,
Gris
ve
arkadaşları,
lupus
antikoagülanın,
provoke
edilmemiş
proksimal
ve
distal
derin
ve
yüzeyel
ven
trombozu
ile
ilişkili
olduğunu
göstermişlerdir.
Diğer
çalışmalarda
da
benzer
sonuçlar
elde
edilmiştir.
Birleşik
Krallık’ta,
Royal
College
of
Gynaecology,
örneğin
APS’nun
klinik
bulgusunu
taşımayan,
aPL
pozitif
hastaların
postpartum
7
gün
tromboprofilaksi
almalarını,
APS
olan
kadınlarda
ise
bu
sürenin
6
haftaya
uzatılmasını
önermektedir
5.
Obstetrik APS’da amaçlar
APS’da
obstetrik
morbiditeyi
önlemek
için
güncel
tedavi
rejimleri,
yukarıda
belirtildiği
gibi
canlı
doğum
oranlarını
%70’in
üzerine
çıkararak
gebelik
sonuçlarını
iyileştirmiştir.
Kadınların
%30’unda
gebelik
komplikasyonları
görülmeye
devam
ettiği
için,
uluslararası
gruplar
halen
APS’lu
kadınlarda
sonuçları
iyileştirmek
için
farklı
seçenekleri
değerlendirmeye
devam
etmektedir.
Tekrarlayan
ilk
trimester
gebelik
kayıplarıyla
giden
dirençli
obstetrik
APS’da
ek
olarak
düşük
doz
steroidlerin
kullanımı
denenmiş
ve
bazı
faydaları
olabileceği
görülmüştür.
Biz
pratiğimizde,
aspirin
ve
DMAH
ile
gebeliğini
devam
etmemiş
hastalara,
gebelik
testi
pozitif
saptandıktan
sonra
12.
gebelik
haftasına
kadar,
tedaviye
günlük
10
mg
prednizolon
ekliyoruz. İntravenöz immünoglobulin, gebelik sonuçlarında anlamlı düzelme sağlanmamıştır.
Pravastatin
hakkındaki
ilgi
çekici
veriler,
bilinen
aPL
ile
ilişkili
preeklampsi
toksemisi
olan
kadınlarda
faydalı
rolü
olduğunu
ileri
sürmektedir.
Bir
olgu
serisinde,
11
hasta
standart
tedaviye
ek
olarak
20
mg
pravastatin
ile
tedavi
edilmiştir,
kontrol
serisindeki
hastalara
ise
sadece
DDA
ve
DMAH
verilmiştir.
Pravastatine
maruz
kalan
tüm
hastalarda,
kontrol
grubuna
kıyasla,
kan
basıncı
yüksekliği
ve
proteinüri
gibi
preeklampsi
bulguları
düzelmiş, plasental perfüzyon bulguları ise ilave bozulma olmaksızın stabil seyretmiştir.
İmmün
modülatör
HCQ’in,
sadece
trombotik
APS’nun
yönetiminde
değil,
gebelik
komplikasyonlarının
önlenmesinde
de
faydalı
etkileri
olabilir.
aPL
ve/veya
APS
olan
gebe
hastaları
içeren
retrospektif
çalışmalarda,
HCQ’in
aPL
ile
ilişkili
olumsuz
gebelik
sonuçlarını
önlemede
iyi
bir
aday
olduğu
hem
bizim
tarafımızdan
hem
diğerleri tarafından kanıtlanmıştır.
Daha
detaylı
bakıldığında,
Mekinian
ve
arkadaşları,
30
APS
hastasından
(ve
35
gebelikten)
oluşan
retrospektif
çok
merkezli
bir
kohort
çalışması
yürütmüşlerdir,
sonuçlara
göre
HCQ
tedavisi
daha
az
ilk
trimester
gebelik
kaybı
(%81’den
%19’a
gerilemiştir,
p<0,05)
ile
ilişkilidir
ve
dirençli
obstetrik
APS’nda
canlı
doğum
oranları
%78’e
yükselmiştir
(p<0,05).
Biz,
96
kadının
170
gebeliğinden
oluşan
retrospektif,
gözlemsel
kohort
çalışmamızda,
HCQ
tedavisinin
artmış
canlı
doğum
oranları
(HCQ
ile
tedavi
edilenlerde
%67,
tedavi
edilmeyenlerde
%57,
p=0,05)
ve
azalmış
gebelik
morbiditesi
(%47’ye
karşı
%63)
ile
ilişkili
olduğunu
gösterdik.
HCQ
alan
hastalarda,
almayanlara
kıyasla
gebelik
süresi
daha
uzundu
(ortalama
27,6
haftaya
karşı
21,5
hafta
(ortalama
6-40
hafta);
p=0,03)
ve
HCQ
tedavisi
alanlarda
10
haftadan
sonra
gebelik
kaybı
daha
nadirdir
(%2’ye
karşı
%11,
p=0,05).
Ayrıca,
HCQ
ile
tedavi
edilen
kadınlarda
kontrol
grubuna
kıyasla,
iskemik
plasenta
aracılı
komplikasyonlar
(preeklampsi,
eklampsi
ve
FGK)
daha
nadirdi
(%2’ye
karşı
%10,9,
p=0,05).
HCQ
tedavisi
alan
grupta
spontan
vajinal
doğum
yapma
oranı
belirgin
derecede
yüksekti
(%37,3’e
karşı
%14,3,
p=0,01).
HCQ
ile
gebelikte
aPL
ilişkili
komplikasyonların
yokluğu
arasındaki
ilişki
multivariabl
analizlerle
doğrulanmıştır
(OR
2,2,
%95
CI
1,2-136,1;
p=0,04).
Yukarıda
bahsedilen
çalışmaların
hiçbirisinde
herhangi
bir
fetal
anomali
gözlenmemiştir.
Prospektif
klinik
çalışmalar
heyecanla
beklenmektedir.
Avrupa’da
randomize
kontrollü
çok
merkezli
çalışma
HYPATIA
(Antifosfolipd
Antikorları
olan
Kadınlarda
Gebelik
Sonuçlarını
İyileştirmek
için
Hidroksiklorokin-Hydroxychloroquine
to
improve
Pregnancy
Outcome
in
women
with
Antiphospholipid
Antibodies),
aPL
olan
kadınlarda
plaseboya
karşı
HCQ’in
rolünü
değerlendirecek
ve
umut
ediyoruz ki bu düzende HCQ kullanımı için en kesin kanıtları sunacaktır.


TJODist
Bülteni

TJOD
İstanbul Şubesi
6.
Özet
APS,
tekrarlayan
ilk
trimester
gebelik
kayıplarının
tedavi
edilebilir
nedenleri
için
en
sık
görülen
edinilmiş
risk
faktörüdür.
aPL,
ölü
doğum,
intrauterin
ölüm,
preeklampsi,
prematür
doğum
ve
fetal
gelişim
kısıtlılığı
gibi
iskemik
plasental
disfonksiyon
durumlar
ve
gebelikte
tromboz
için
risk
artışıyla
beraberdir.
Obstetrik
APS’nun
güncel
standart
tedavisi
aspirin
ve
DMAH’e
dayanmaktadır.
Gebelik
sonuçlarını
iyileştirmeyi
amaçlayan
yeni
yaklaşımlar immün modülatör HCQ’i içermektedir.


TJODist
Bülteni